题目内容
9.已知氟元素与氯元素位于元素周期表的同一纵行,且氟原子得电子能力比氯原子强,试写出氟化钠的化学式NaF.分析 根据化合物的化学式的写法来分析,正价元素在前,负价元素在后,正负化合价的代数和为零.
解答 解:氟元素的原子最外层有7个电子,易得到一个电子而显-1价,钠元素最外层有1个电子,在化学反应中易失去一个电子而显+1价,故化学式为NaF.
故填:NaF.
点评 掌握元素化合价的推断方法以及化合物的化学式的写法是解题的关键.

练习册系列答案
相关题目
19.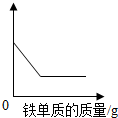 在盛有一定质量硫酸铜溶液的小烧杯中,逐渐加入铁粉,直至过量.如图横坐标表示加入铁粉的质量,根据图象判断纵坐标可能表示( )
在盛有一定质量硫酸铜溶液的小烧杯中,逐渐加入铁粉,直至过量.如图横坐标表示加入铁粉的质量,根据图象判断纵坐标可能表示( )
 在盛有一定质量硫酸铜溶液的小烧杯中,逐渐加入铁粉,直至过量.如图横坐标表示加入铁粉的质量,根据图象判断纵坐标可能表示( )
在盛有一定质量硫酸铜溶液的小烧杯中,逐渐加入铁粉,直至过量.如图横坐标表示加入铁粉的质量,根据图象判断纵坐标可能表示( )| A. | 小烧杯中所有物质的总质量 | B. | 小烧杯中溶液的总质量 | ||
| C. | 小烧杯中离子的总数目 | D. | 小烧杯中固体中的总质量 |
20.下列物质的用途与性质对应不正确的是( )
| 物 质 | 用 途 | 性 质 | |
| A | 氧气 | 作火箭发射的助燃剂 | 氧气具有可燃性 |
| B | 熟石灰 | 改良酸性土壤 | 熟石灰能与酸发生中和反应 |
| C | 小苏打 | 治疗胃酸过多 | 小苏打能与盐酸反应 |
| D | 氮气 | 焊接金属时做保护气 | 氮气的化学性质不活泼 |
| A. | A | B. | B | C. | C | D. | D |
11.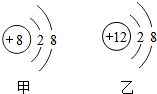 如图为甲、乙两种微粒结构示意图,下列有关叙述正确的是( )
如图为甲、乙两种微粒结构示意图,下列有关叙述正确的是( )
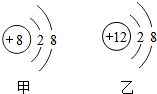 如图为甲、乙两种微粒结构示意图,下列有关叙述正确的是( )
如图为甲、乙两种微粒结构示意图,下列有关叙述正确的是( )| A. | 它们属于同种元素 | B. | 它们构成的单质为稀有气体 | ||
| C. | 它们的核外电子数不同 | D. | 甲表示阴离子,乙表示阳离子 |
9.2014年,大运河申遗成功,保护大运河人人有责.二甲基三硫(C2H6S3)是经常造成水污染的主要物质之一.关于二甲基三硫(C2H6S3),下列说法正确的是( )
| A. | 二甲基三硫由C、H、S原子构成 | |
| B. | 二甲基三硫中C、H、S元素的质量比为2:6:3 | |
| C. | 二甲基三硫的相对分子质量为126 g | |
| D. | 二甲基三硫属于有机物 |
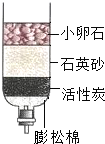 水与人类的生活和生产密切相关.
水与人类的生活和生产密切相关.