题目内容
3.“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质,工业提纯粗盐的工艺流程如图所示.请回答: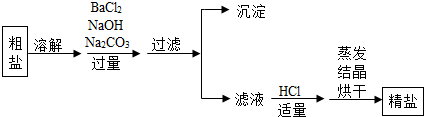
(1)在溶解、过滤、蒸发的过程中均用到了同一玻璃仪器,该仪器在蒸发时的作用是搅拌,防止局部温度过高,造成液滴飞.
(2)用两个化学方程式表示加入碳酸钠的目的.BaCl2+Na2CO3═BaCO3↓+2NaCl、CaCl2+Na2CO3═CaCO3↓+2NaCl.
(3)在滤液中,即使过量加稀盐酸对提纯精盐没有影响的原因是盐酸具有挥发性.
分析 (1)根据溶解、过滤、蒸发所需的仪器,进行分析解答.
(2)根据碳酸钠能与过量的氯化钡反应生成碳酸钡沉淀和氯化钠,能与氯化钙反应生成碳酸钙沉淀和氯化钠,进行分析解答.
(3)根据盐酸具有挥发性,进行分析解答.
解答 解:(1)溶解、过滤、蒸发操作中都要用到的同一玻璃仪器是玻璃棒,该仪器在蒸发时的作用是搅拌,防止局部温度过高,造成液滴飞溅.
(2)碳酸钠能与过量的氯化钡反应生成碳酸钡沉淀和氯化钠,能与氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式分别是BaCl2+Na2CO3═BaCO3↓+2NaCl、CaCl2+Na2CO3═CaCO3↓+2NaCl.
(3)在滤液中,即使过量加稀盐酸对提纯精盐没有影响的原因是盐酸具有挥发性.
故答案为:(1)搅拌,防止局部温度过高,造成液滴飞;(2)BaCl2+Na2CO3═BaCO3↓+2NaCl、CaCl2+Na2CO3═CaCO3↓+2NaCl;(3)盐酸具有挥发性.
点评 本题难度不大,掌握粗盐提纯的原理、盐的化学性质、盐酸具有挥发性等是正确解答本题的关键.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
13.下列物质量中氮元素的含量最高的是( )
| A. | NO | B. | N2O3 | C. | NO2 | D. | N2O5 |
12.化学兴趣小组欲探究自己使用的某品牌牙膏的主要成分.
【查阅资料】
(1)牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质.
(2)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2.
(3)牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体.
(4)SiO2不溶于水,也不与盐酸反应.Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O.偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应.
(5)相关物质的溶解性表:
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3.
猜想2:摩擦剂的成分为SiO2和CaCO3.
猜想3:摩擦剂的成分为SiO2和Al(OH)3.
设计实验】
【实验结论】经过实验验证,猜想1成立.
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为牙膏样品中部分固体溶解,向上层清夜中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解,依据该现象可以判断摩擦剂中一定含有氢氧化铝.
【查阅资料】
(1)牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质.
(2)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2.
(3)牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体.
(4)SiO2不溶于水,也不与盐酸反应.Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O.偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应.
| 物质 | Al(OH)3 | NaAlO2 | AlCl3 |
| 溶解性 | 不溶 | 溶 | 溶 |
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3.
猜想2:摩擦剂的成分为SiO2和CaCO3.
猜想3:摩擦剂的成分为SiO2和Al(OH)3.
设计实验】
| 实验步骤 | 预期实验现象 | 预期实验结论 |
组装下图装置进行实验.取少量摩擦剂于锥形瓶中,加入适量的稀盐酸.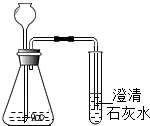 | 固体全部溶解,有气泡,石灰水变混浊 | 则猜想1成立 锥形瓶中发生的化学反应方程式为Al(OH)3+3HCl=AlCl3+3H2O CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 摩擦剂部分溶解 石灰水无明显变化 | 则猜想3成立 |
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为牙膏样品中部分固体溶解,向上层清夜中滴加稀盐酸时开始无现象,之后有固体产生,最后固体溶解,依据该现象可以判断摩擦剂中一定含有氢氧化铝.
13.下列叙述中没有化学变化的是( )
| A. | 蜡烛燃烧 | B. | 钢铁锈蚀 | C. | 呼吸作用 | D. | 干冰升华 |
 某同学设计如图所示的装置.将铁丝放在潮湿的空气中,一周后,除观察到铁丝生锈,还观察到的现象是烧杯中的水沿导管上升;打开K后,观察到铁锈消失,写出该反应的化学方程式Fe2O3 +6HCl=2FeCl3+3H2O;随着盐酸的滴加,过一会观察到烧杯内的导管口有气泡冒出,请解释产生该现象的原因盐酸和铁反应生成生成氢气,从导管口逸出.
某同学设计如图所示的装置.将铁丝放在潮湿的空气中,一周后,除观察到铁丝生锈,还观察到的现象是烧杯中的水沿导管上升;打开K后,观察到铁锈消失,写出该反应的化学方程式Fe2O3 +6HCl=2FeCl3+3H2O;随着盐酸的滴加,过一会观察到烧杯内的导管口有气泡冒出,请解释产生该现象的原因盐酸和铁反应生成生成氢气,从导管口逸出.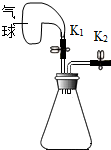 某同学利用如图装置进行如下实验(装置气密性良好).
某同学利用如图装置进行如下实验(装置气密性良好).