题目内容
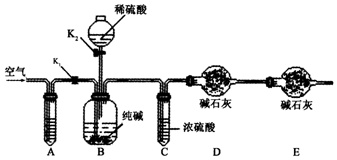
17.某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:①按图连接装置,并检查气密性;②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83.4g;③准确称得6g纯碱样品并放入容器B中;④关上K1,打开K2,缓缓滴入稀硫酸,至不再产生气泡为止;⑤关上K2,打开K1,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g.
试回答:
(1)已知装置A中试剂为碱性溶液,其作用是除去空气中的二氧化碳.
(2)实验步骤⑤鼓入空气的目的是把装置中的二氧化碳排出,让装置D吸收,使结果更准确.
(3)若没有C装置,则会导致测定结果偏大(填“偏大”或“偏小”).
(4)E装置的作用是防止空气中的二氧化碳进入D装置.
(5)根据实验中测得的有关数据,计算出纯碱样品碳酸钠的质量分数为多少?(计算结果保留一位小数).
(6)经精确测定,样品中碳酸钠的实际质量分数略小于上述所求数值,其原因可能是装置中有一定量的空气,所含的CO2也会进入D中.
分析 本题考查的是盐的化学性质,由题目的信息可知:已知装置A中试剂为碱性溶液,其作用是除去空气中的二氧化碳;实验步骤⑤鼓入空气的目的是:把装置中的二氧化碳排出,让装置D吸收,使结果更准确;若没有C装置,则会导致测定结果偏大,因为水蒸气也会被D装置吸收;E装置的作用是:防止空气中的二氧化碳进入D装置;根据化学方程式的计算要准确.
解答 解:(1)已知装置A中试剂为碱性溶液,其作用是除去空气中的二氧化碳;故答案为:除去空气中的二氧化碳;
(2)实验步骤⑤鼓入空气的目的是:把装置中的二氧化碳排出,让装置D吸收,使结果更准确;故答案为:把装置中的二氧化碳排出,让装置D吸收,使结果更准确;
(3)若没有C装置,则会导致测定结果偏大,因为水蒸气也会被D装置吸收;故答案为:偏大;
(4)E装置的作用是:防止空气中的二氧化碳进入D装置;故答案为:防止空气中的二氧化碳进入D装置;
(5)二氧化碳的质量=85.6g-83.4g=2.2g,设纯碱样品碳酸钠的质量分数为x,
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
106 44
6g•x 2.2g
$\frac{106}{44}=\frac{6g•x}{2.2g}$
x≈88.3%;
答:纯碱样品碳酸钠的质量分数为88.3%;
(6)由于在装置中不可避免的要存有残留的空气,而空气中的二氧化碳被D装置吸收,而导致测量结果偏大,故本题答案为:装置中有一定量的空气,所含的CO2也会进入D中.
点评 本考点属于盐的化学性质和有关的计算等,盐的化学性质有四个:盐与金属反应、盐与酸反应、盐与碱反应、盐与盐反应.解决本考点需要根据实验现象,综合分析,从而得出正确的结论,有关的计算要准确.此考点主要出现在选择题和实验题中.

 名校课堂系列答案
名校课堂系列答案| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
| 食盐种类 | 食盐A | 食盐B |
| 主要成分的含量 | (以钠元素质量计) 35.1g/100g | (以NaCl质量计) 93.0g/100g |
(1)加碘盐是通过加入KIO3的方法制成的,KIO3中碘元素的化合价为+5.
(2)NaCl中钠元素质量分数以39%计,则100克食盐A中氯化钠的质量是90克,100克食盐B中钠元素的质量是36.27克.
| A. |  | B. | 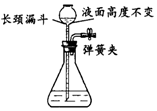 | ||
| C. | 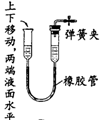 | D. |  |
 A、B两种化合物的溶解度曲线如图.现要用结晶法从A、B混和物中提取A.(不考虑A、B共存时,对各自溶解度的影响.)
A、B两种化合物的溶解度曲线如图.现要用结晶法从A、B混和物中提取A.(不考虑A、B共存时,对各自溶解度的影响.)