题目内容
硝酸钾溶液中含有少量氯化钠,若得到较为纯净的硝酸钾晶体,可采用的下列方法是( )
A.过滤 B.蒸发溶剂
C.降温结晶 D.蒸馏
选C。过滤只能分离液体与不溶性固体,A方法不可;将溶液蒸发,仍得到含食盐的硝酸钾,B方法不可;降温结晶,即降低热饱和溶液的温度,因氯化钠的量少,氯化钠的溶解度随温度变化不大,故析出的晶体可视为纯净的硝酸钾,C方法可以;蒸馏时,固体仍将剩余在母液中,不可能得到纯净的硝酸钾晶体,D方法不可。

一节一号干电池烂在地里,能使1m2的土壤永久失去利用价值;一粒纽扣电池可使600t水受到污染,相当于一个人一生的饮水量.许多有识之士正在研究废旧电池的有效回收再利用技术.图1为干电池示意图.
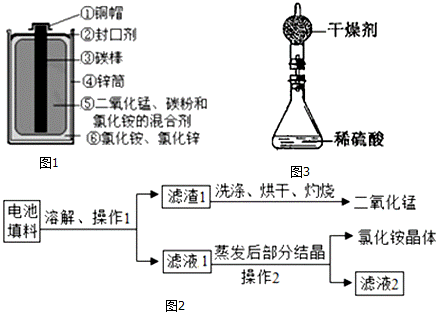
【物质归类】将回收的废干旧电池进行分离归类
(1)可以得到的单质有(用化学式表示,下同) ,
氧化物有 .
某化学兴趣小组回收利用废旧干电池并进行相关实验探究.
【实验探究1】回收填料中的二氧化锰和氯化铵
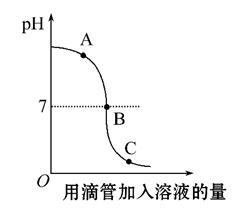
查阅资料:干电池示意图中⑤和⑥为填料,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如图2所示.
(2)操作1和操作2的名称都是 ,该操作中玻璃棒的作用是 .
(3)灼烧滤渣l的目的是 .
【实验探究2】探究影响锌与稀硫酸反应快慢的因素
(4)反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如下表.
| 实验编号 | 试剂 | 前10 min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 mL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
①比较实验a和实验b,可以得到的结论是 .
②为了研究硫酸浓度对反应快慢的影响,需比较实验 和实验 (填编号).
③控制其他条件相同,需控制的条件是 (例举一种条件即可).
【实验探究3】利用锌皮和稀硫酸制取氢气,并测定锌皮中锌的质量分数
(5)制取氢气的实验操作有:
a.收集气体;b.向锥形瓶里装锌皮;c.连接仪器,检查装置气密性;d.向长颈漏斗中注入稀硫酸;e.装配仪器.
正确的操作顺序为 .
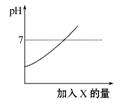
(6)测定锌皮中锌的质量分数:已知该锌皮中含有少量杂质铁,将该锌皮放入如图3所示的盛有稀硫酸的锥形瓶中,多次实验后,取平均值所得数据如表:
| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌皮质量 | |
| 342.1g | 16g | 357.7g |
若不考虑干燥剂吸收空气中的水蒸气,请分析计算:
①根据质量守恒定律求生成氢气的质量为 g.
②该合金中锌的质量为 g,锌皮中锌的质量分数为 %.
 向稀盐酸中逐渐加入试剂X后,溶液的pH变化情况如图所示。试剂X是下列物质中的( )
向稀盐酸中逐渐加入试剂X后,溶液的pH变化情况如图所示。试剂X是下列物质中的( )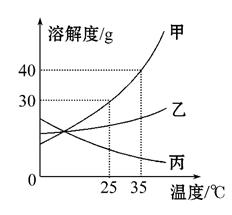
 就是不能再溶解任何物质的溶液
就是不能再溶解任何物质的溶液