题目内容
3.小华采用加热氯酸钾的方法制取氧气,错把高锰酸钾当作二氧化锰放入氯酸钾内,其结果与只加氯酸钾相比,正确的是( )| A. | 反应速率不变,生成氧气的质量不变 | |
| B. | 反应速率加快,生成氧气的质量不变 | |
| C. | 反应速率加快,生成氧气的质量增加 | |
| D. | 高锰酸钾在反应中起催化剂的作用 |
分析 高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,二氧化锰可作为氯酸钾制取氧气的催化剂,加快化学反应速率;据此进行分析判断.
解答 解:A、高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰和氧气,生成的二氧化锰可作氯酸钾反应的催化剂,可加快化学反应速率;生成氧气的质量与单纯加热氯酸钾相比,质量增加,故选项说法错误.
B、高锰酸钾分解可生成氧气,生成氧气的质量与单纯加热氯酸钾相比,质量要增加,故选项说法错误.
C、生成的二氧化锰可作氯酸钾反应的催化剂,可加快化学反应速率,所以反应速率加快,生成氧气质量增加,故选项说法正确.
D、高锰酸钾分解生成的二氧化锰可作氯酸钾反应的催化剂,可加快化学反应速率,故选项说法错误.
故选C.
点评 本题难度不大,掌握高锰酸钾和氯酸钾制取氧气的反应原理及二氧化锰在氯酸钾反应中的作用并能灵活运用是正确解答本题的关键.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
13.实验中的下列操作正确的是( )
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 | |
| C. | 用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | 天然气泄漏,立即关闭阀门并开窗通风 |
14.以下实验基本操作正确的是( )
| A. | 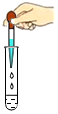 用滴管滴液 | B. |  加热液体 | C. | 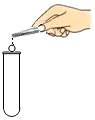 向试管加固体 | D. |  量取液体 |
18.有一种只含SiO2杂质(SiO2不溶于水,也不与盐酸反应)的石灰石样品.某学生想测定该样品中碳酸钙的质量分数,他取用12g样品,把100g稀盐酸平分4次加入,充分反应后剩余固体的质量依次记录于下表
(1)样品中碳酸钙的质量分数.
(2)2g样品与稀盐酸反应时,恰好用去稀盐酸的质量.
(3)稀盐酸的质量分数.
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 反应后烧杯中物质的总质量/g | 35.2 | 58.4 | 82.6 | 107.6 |
(2)2g样品与稀盐酸反应时,恰好用去稀盐酸的质量.
(3)稀盐酸的质量分数.
15.无铅汽油一般是加入甲基叔丁基醚【CH3OC(CH3)3】作为高辛烷值组分.下列关于甲基叔丁基醚叙述错误的是( )
| A. | 甲基叔丁基醚属于化合物 | |
| B. | 甲基叔丁基醚的相对分子质量为88 | |
| C. | 甲基叔丁基醚中碳元素的质量分数约为68.2% | |
| D. | 一个甲基叔丁基醚分子是由5个碳原子、9个氢原子和1个氧原子构成的 |
12.粗盐的杂质主要是氯化镁(能溶于水),工业上常把粗盐粉碎后用饱和的食盐水浸泡,在过滤出食盐,对此,下列结论正确的( )
| A. | 浸洗前后,被浸洗的粗盐中氯化镁的含量基本不变 | |
| B. | 浸洗前后,饱和食盐水中氯化钠的质量基本不变 | |
| C. | 浸洗用的饱和食盐水可以无数次的使用下去 | |
| D. | 浸洗后,食盐水中氯化钠的质量增大 |
13.对下列事实解释不正确的是( )
| 选项 | 事 实 | 解 释 |
| A | 一滴水中大约有1.67×1021个水分子 | 分子很小 |
| B | 敞口容器中的酒精逐渐减少 | 分子是不断运动的 |
| C | 体温计中的水银(汞)热胀冷缩 | 原子的体积热胀冷缩 |
| D | 炎热的夏天自行车车胎容易爆裂 | 夏天温度高,分子间隔变大 |
| A. | A | B. | B | C. | C | D. | D |