题目内容
1.人类的生产生活离不开金属,铁是当前年产量最高的金属.(1)国际上推广使用中国铁锅,因为铁锅能为人补铁,人体缺铁会引起缺铁性贫血;
(2)我国古代发明了“曾清(即硫酸铜)得铁化为铜”的湿法炼铜法,请用化学方程式表示反应原理:Fe+CuSO4=FeSO4+Cu;
(3)将铁粉投入含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有铜和银.
分析 (1)根据铁元素在人体所起的作用进行分析;
(2)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(3)根据金属活动顺序表知:铁>铜>银,所以加入铁粉,首先铁粉和硝酸银溶液反应,置换出单质银,如果铁粉足量可以再继续和硝酸铜反应置换出铜,若滤液中只含有一种溶质,说明溶液中只含有硝酸亚铁,滤渣中一定含有铜和银,可能含有铁进行分析.
解答 解:(1)铁锅能为人补铁,人体缺铁会引起缺铁性贫血;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
(3)由金属活动顺序表知:铁>铜>银,所以加入铁粉,首先铁粉和硝酸银溶液反应,置换出单质银,如果铁粉足量可以再继续和硝酸铜反应置换出铜,若滤液中只含有一种溶质,说明溶液中只含有硝酸亚铁,滤渣中一定含有铜和银,可能含有铁.
故答案为:(1)缺铁性贫血;
(2)Fe+CuSO4=FeSO4+Cu;
(3)铜,银.
点评 本题主要考查了学生对金属活动顺序表的运用以及半待定量(如一定量、过量、少量等)概念的理解和掌握.

练习册系列答案
相关题目
9.把下列物质溶于水中,一定能得到无色溶液的是( )
| A. | NaOH、MgSO4、BaCl2、HNO3 | B. | KNO3、Na2CO3、HCl、NaOH | ||
| C. | HNO3、CuCl2、AgNO3、KOH | D. | KMnO4、NaNO3、HCl、MgSO4 |
13.下列除去杂质(在括号内)选用的方法中不正确的是( )
| A. | CO气体(CO2)→通入NaOH溶液中 | |
| B. | NaCl固体(泥沙)→加水溶解、过滤、蒸发 | |
| C. | KCl溶液(K2CO3)→加适量稀硫酸 | |
| D. | Cu粉(Fe)→用磁铁吸引 |
10.下列说法中正确的是( )
| A. | 空气中氮气体积分数约为78% | |
| B. | “碘盐”中的“碘”指的是离子 | |
| C. | 通常把pH<7的降水称为酸雨 | |
| D. | 氯化铵可与草木灰(含碳酸钾)混合施用 |

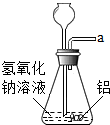 兴趣小组在实验时,某同学误将氢氧化钠溶液当成酸滴加到金属中,结果发现也有气泡产生,他猜想该气体可能是氧气、氢气或二氧化碳.
兴趣小组在实验时,某同学误将氢氧化钠溶液当成酸滴加到金属中,结果发现也有气泡产生,他猜想该气体可能是氧气、氢气或二氧化碳.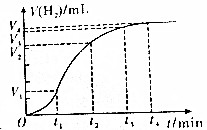 进行锌与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳锌与稀盐酸反应速率的变化规律锌与稀盐酸反应的速率先慢后快最后又慢,结合上述探究解释曲线变化的原因开始时反应物浓度最大,随着反应的进行浓度降低,但反应放热,温度逐渐升高,所以反应速率逐渐增大,随着反应的进行,浓度逐渐减小,浓度因素大于温度因素,反应速率逐渐减小.
进行锌与稀盐酸反应时,试管外壁发烫,并测得实验过程中生成氢气的体积随时间变化的曲线如图乙所示,根据曲线归纳锌与稀盐酸反应速率的变化规律锌与稀盐酸反应的速率先慢后快最后又慢,结合上述探究解释曲线变化的原因开始时反应物浓度最大,随着反应的进行浓度降低,但反应放热,温度逐渐升高,所以反应速率逐渐增大,随着反应的进行,浓度逐渐减小,浓度因素大于温度因素,反应速率逐渐减小.