题目内容
4.下列物质与水混合,温度明显降低的是( )| A. | CaO | B. | 浓H2SO4 | C. | NaOH | D. | NH4NO3 |
分析 根据常见物质溶于水的吸热与放热现象、溶液温度的变化情况进行分析解答即可.
解答 解:物质在溶解时经常伴随有吸热或放热现象,如氢氧化钠固体、浓硫酸溶于放出大量的热,温度升高;硝酸铵固体溶于水吸热,温度降低.
A、氧化钙溶于水放热,溶液温度明显升高,故选项错误.
B、浓硫酸溶于水放热,溶液温度明显升高,故选项错误.
C、氢氧化钠溶于水放热,溶液温度明显升高,故选项错误.
D、硝酸铵溶于水吸热,溶液温度明显降低,故选项正确.
故选D
点评 本题难度不大,掌握常见物质溶于水的吸热与放热现象、温度变化情况是正确解答本题的关键.

练习册系列答案
相关题目
15.40g10%的氢氧化钠溶液和40g10%的稀盐酸充分混合,混合后的溶液与下列物质能反应的是( )
| A. | Na2CO3溶液 | B. | NaCl溶液 | C. | 稀硫酸 | D. | CO2气体 |
12.用H2O、HgO、H2O2三种物质都可制得氧气,说明这三种物质的组成中都含有( )
| A. | 氧元素 | B. | 氧气 | C. | 氧分子 | D. | 氧离子 |
19.如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )


| A. | t1℃时,甲的溶解度大于乙的溶解度 | |
| B. | 加入甲或升温都可以使接近饱和的甲溶液变为饱和溶液 | |
| C. | t2℃时,甲、乙各40 g分别加入到100g水中,均能得到不饱和溶液 | |
| D. | t2℃时,甲、乙各40 g分别加入到100g水中,再升温至t3℃,两种溶液中溶质质量分数相等 |
9.下列有关CO2性质的描述中,错误的是( )
| A. | 密度比空气小 | B. | 能溶于水 | C. | 不燃烧 | D. | 能与碱反应 |
16.地壳中含量最多的元素是( )
| A. | 硅 | B. | 铝 | C. | 铁 | D. | 氧 |
14.下列关于空气和氧气的说法正确的是( )
| A. | 磷在空气中燃烧产生大量白色烟雾 | |
| B. | 农药和化肥过量施用不会造成空气污染 | |
| C. | “高山反应”是因为高海拔地区空气中没有氧气 | |
| D. | 氧气和臭氧化学性质不同的原因是分子构成不同 |
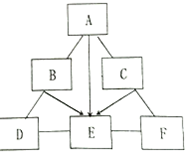 A、B、C、D、E、F分别是碳、二氧化碳、氧化铁、氢氧化钙溶液,碳酸钠溶液和稀盐酸中的一种物质,用“-”表示二者能发生化学反应,用“→”表示一种物质能进一步转化为另一种物质(反应条件已略去)如图是六种物质间的部分反应和转化关系,请回答下列问题:
A、B、C、D、E、F分别是碳、二氧化碳、氧化铁、氢氧化钙溶液,碳酸钠溶液和稀盐酸中的一种物质,用“-”表示二者能发生化学反应,用“→”表示一种物质能进一步转化为另一种物质(反应条件已略去)如图是六种物质间的部分反应和转化关系,请回答下列问题: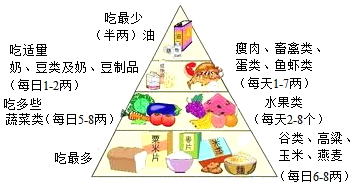 均衡饮食是健康的基础.右图是中国居民的膳食宝塔,由下至上各层所示食品中富含的营养素分别为糖类、维生素、蛋白质、油脂.
均衡饮食是健康的基础.右图是中国居民的膳食宝塔,由下至上各层所示食品中富含的营养素分别为糖类、维生素、蛋白质、油脂.