题目内容
15.下表列出了20℃时KNO3溶解实验的一组数据:| 实验序号 | 水的质量/g | 所加KNO3的质量/g | 所得溶液的质量/g |
| ① | 10 | 2.5 | 12.5 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 3.5 | m |
| ④ | 10 | 4 | 13.2 |
| A. | ①②所得的溶液是不饱和溶液 | B. | ③中m=13.2 | ||
| C. | 20℃时KNO3的溶解度为32g | D. | ④所得溶液的溶质质量分数为32% |
分析 根据表格中的实验数据,结合溶液质量与溶剂质量和溶质质量之和的关系来分析溶液的状态.
解答 解:在实验①和实验②中溶液质量等于溶剂质量+溶质的质量,而实验③和④中溶液质量小于溶剂质量+溶质质量,
则实验③和④中都有固体不溶解,即实验③和④得到的都是硝酸钾的饱和溶液,实验③中硝酸钾能溶解3.2g;故m=13.2g;①②得到的是不饱和溶液;由实验④可知,溶解的溶质质量为3.2g;即该温度下,10g水中溶解3.2g硝酸钾恰好饱和,则该温度下硝酸钾的溶解度为32g,此时饱和溶液的溶质质量分数=$\frac{32}{132}$×100%=24.2%.故D错误.
故答案选:D.
点评 本题考查饱和溶液的判断和溶解度的简单计算,学生利用在该条件下有固体不能继续溶解来判断是否为饱和溶液是解答的关键.

练习册系列答案
相关题目
5.舞台上经常用喷撒干冰(固态二氧化碳)的方法制造白雾渲染气氛,对“白雾”的形成.小星的解释是:(1)干冰升华吸热使周围环境温度降低,(2)气态二氧化碳液化形成白雾.以上解释中( )
| A. | 第一句话存在科学性错误 | B. | 第二句话存在科学性错误 | ||
| C. | 两句话都存在科学性错误 | D. | 两句话都没有科学性错误 |
10.如图是一个化学反应的微观示意图,从示意图获取的信息正确的是( )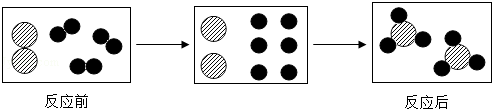

| A. | 反应前后分子种类不发生改变 | |
| B. | 反应前后原子的种类与数目不发生改变 | |
| C. | 反应前两种分子的个数比是1:2 | |
| D. | 该反应的基本类型是分解反应 |
20.以科学原理和实验事实为依据进行推理是学习化学的一种重要方法.下列推理得出的相关结论合理的是
( )
( )
| A. | 原子在化学变化中不能再分,所以分子在化学变化中也不能再分 | |
| B. | 化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物 | |
| C. | 溶液是均一、稳定的物质,所以均一、稳定的物质一定是溶液 | |
| D. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
5.毒品大麻(其化学式为C21H30O2)对人体产生起大的危害.有关大麻的说法正确的是( )
| A. | 大麻由53个原子构成 | B. | 大麻中碳元素的质量分数为8% | ||
| C. | 大麻中各元素的质量比为21:30:2 | D. | 每个大麻分子里含有5个氢分子 |
 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答:
