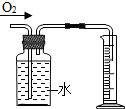
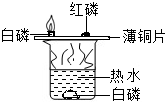
题目内容
某实验小组对“高温煅烧石灰石是否完全分解”进行如下研究:
①电子天平称量时,若需要直接显示石灰石的质量,在放称量纸或烧杯后,需要进行的操作是 (填“校准”、“归零”或“去皮”).
②在1、2、3、4的四个步骤中,根据步骤 (填序号,下同),可得出“石灰石有部分已经分解”;根据步骤 ,可得出“石灰石没有完全分解”.
| 步骤 | 实 验 过 程 | 简 答 |
| 1 | 取一小块石灰石,用电子天平准确称量 | |
| 2 | 将其在酒精喷灯上灼烧一段时间后,表面疏松,待冷却后再称量,固体质量 | 反应的化学方程式: |
| 3 | 将一部分灼烧过的石灰石放入试管中,滴加水,搅拌片刻,往溶液中滴入酚酞试液. | 酚酞试液显 |
| 4 | 将一部分灼烧过的石灰石放入试管中,滴加盐酸,发现有气泡产生. |
②在1、2、3、4的四个步骤中,根据步骤
考点:盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:1、根据碳酸钙高温分解分析,及质量守恒定律分析;
2、氧化钙与水反应生成氢氧化钙,溶液显碱性;
①根据电子天平称量的操作分析;
②根据实验步骤的现象分析.
2、氧化钙与水反应生成氢氧化钙,溶液显碱性;
①根据电子天平称量的操作分析;
②根据实验步骤的现象分析.
解答:解:1、碳酸钙高温能分解生成氧化钙和二氧化碳,反应的化学方程式:CaCO3
CaO+CO2↑;由质量守恒定律可知:参加反应的碳酸钙的质量与生成的氧化钙和二氧化碳的质量总和相等,由于二氧化碳逸出,所以待冷却后再称量,固体质量减小;
2、氧化钙与水反应生成氢氧化钙,溶液显碱性,往溶液中滴入酚酞试液会变红色;
①电子天平称量时,若需要直接显示石灰石的质量,在放称量纸或烧杯后,需要去除纸或烧杯的质量,所以要去皮.
②由质量守恒定律可知:参加反应的碳酸钙的质量与生成的氧化钙和二氧化碳的质量总和相等,由于二氧化碳逸出,所以待冷却后再称量,固体质量减小;所以步骤2可得出“石灰石有部分已经分解”;将一部分灼烧过的石灰石放入试管中,滴加水,搅拌片刻,往溶液中滴入酚酞试液变红色,说明生成了氧化钙,所以步骤3可得出“石灰石有部分已经分解”;
将一部分灼烧过的石灰石放入试管中,滴加盐酸,发现有气泡产生,说明生成固体中含有碳酸钙,所以步骤4可得出“石灰石没有完全分解”.
故答案为:
①去皮
②2(3;2或3;2和3均可);4
| ||
2、氧化钙与水反应生成氢氧化钙,溶液显碱性,往溶液中滴入酚酞试液会变红色;
①电子天平称量时,若需要直接显示石灰石的质量,在放称量纸或烧杯后,需要去除纸或烧杯的质量,所以要去皮.
②由质量守恒定律可知:参加反应的碳酸钙的质量与生成的氧化钙和二氧化碳的质量总和相等,由于二氧化碳逸出,所以待冷却后再称量,固体质量减小;所以步骤2可得出“石灰石有部分已经分解”;将一部分灼烧过的石灰石放入试管中,滴加水,搅拌片刻,往溶液中滴入酚酞试液变红色,说明生成了氧化钙,所以步骤3可得出“石灰石有部分已经分解”;
将一部分灼烧过的石灰石放入试管中,滴加盐酸,发现有气泡产生,说明生成固体中含有碳酸钙,所以步骤4可得出“石灰石没有完全分解”.
故答案为:
| 步骤 | 实 验 过 程 | 简 答 | ||||
| 1 | 取一小块石灰石,用电子天平准确称量 | |||||
| 2 | 将其在酒精喷灯上灼烧一段时间后,表面疏松,待冷却后再称量,固体质量减小(填“增大”、“减小”或“不变”) | 反应的化学方程式:CaCO3
| ||||
| 3 | 将一部分灼烧过的石灰石放入试管中,滴加水,搅拌片刻,往溶液中滴入酚酞试液. | 酚酞试液显红色. | ||||
| 4 | 将一部分灼烧过的石灰石放入试管中,滴加盐酸,发现有气泡产生. |
②2(3;2或3;2和3均可);4
点评:此题为CaCO3和CaO性质的探究. 常见的CaO、Ca(OH)2、CaCO3性质的探究还有:例如松花蛋的制作原理中的化学方程式,裹在皮蛋壳外固体物质成分的探究,锅炉水垢的成分的探究,珍珠真假的辨认等

练习册系列答案
相关题目
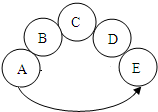 A、B、C、D、E是初中化学中常见的五种物质,其中A、B、C、D、E分别是硫酸、氢氧化钠溶液、氧化铁、一氧化碳、二氧化碳中的一种物质.A与E中含有相同的元素,用五个圆表示五种物质,用两圆相切表示两种物质可以发生化学反应,“→”表示是两物质间的转化关系,由A转化为E是放热反应.(部分反应物、生成物和反应条件已略去).请回答下列问题:
A、B、C、D、E是初中化学中常见的五种物质,其中A、B、C、D、E分别是硫酸、氢氧化钠溶液、氧化铁、一氧化碳、二氧化碳中的一种物质.A与E中含有相同的元素,用五个圆表示五种物质,用两圆相切表示两种物质可以发生化学反应,“→”表示是两物质间的转化关系,由A转化为E是放热反应.(部分反应物、生成物和反应条件已略去).请回答下列问题: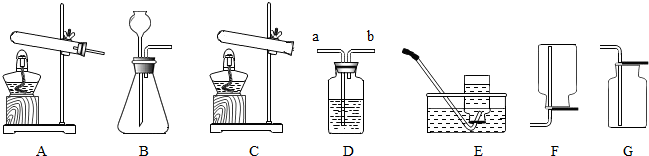
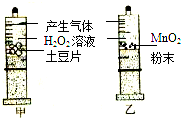 小陈同学将一片土豆片放入过氧化氢溶液中,发现过氧化氢溶液的分解速率加快,查阅资料后,他知道土豆中含有过氧化氢酶,是一种生物催化剂.同时他联想到初二时学习氧气的制取时,可用二氧化锰作催化剂分解过氧化氢溶液,于是他设计了如图实验:常温下,将适量的土豆和二氧化锰粉末事先放入甲乙两只注射器中,然后在注射器中抽入相同体积和溶质质量分数的过氧化氢溶液,密封后观察注射器中气泡的产生速率.
小陈同学将一片土豆片放入过氧化氢溶液中,发现过氧化氢溶液的分解速率加快,查阅资料后,他知道土豆中含有过氧化氢酶,是一种生物催化剂.同时他联想到初二时学习氧气的制取时,可用二氧化锰作催化剂分解过氧化氢溶液,于是他设计了如图实验:常温下,将适量的土豆和二氧化锰粉末事先放入甲乙两只注射器中,然后在注射器中抽入相同体积和溶质质量分数的过氧化氢溶液,密封后观察注射器中气泡的产生速率. 为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小吴设计了一套实验装置(如图).他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量和质量分数)进行反应.在相同条件下测定不同时间内收集 到的气体体积,实验记录如下表:
为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小吴设计了一套实验装置(如图).他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量和质量分数)进行反应.在相同条件下测定不同时间内收集 到的气体体积,实验记录如下表: