题目内容
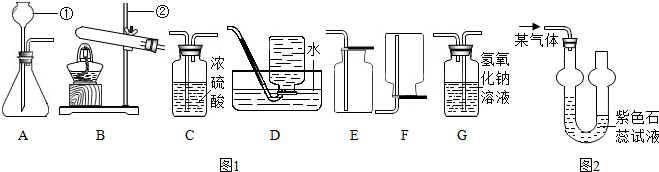
 (1)下列实验均用到水,其中水仅作为溶剂的是
(1)下列实验均用到水,其中水仅作为溶剂的是A.配制0.9%的生理盐水 B.生石灰变成熟石灰
C.浓硫酸稀释
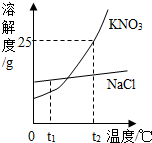
(2)如图为KNO3和NaCl两种物质的溶解度曲线.
①两种物质溶解度的变化受温度影响较小的是
②t2℃时,将30g KNO3固体投入50g水中,充分溶解后可得到 KNO3
(3)工业上将硝酸钾和氯化钠的热混合溶液(两者均已达饱和)冷却至室温,析出晶体.对析出的晶体和剩余溶液描述正确的是
A.剩余溶液一定是KNO3饱和溶液 B.剩余溶液一定是NaCl饱和溶液
C.上述方法可以将两者完全分离 D.析出的晶体中只含有KNO3.
考点:溶液、溶质和溶剂的相互关系与判断,浓硫酸的性质及浓硫酸的稀释,固体溶解度曲线及其作用,晶体和结晶的概念与现象,生石灰的性质与用途
专题:溶液、浊液与溶解度,常见的酸 酸的通性,常见的碱 碱的通性
分析:(1)根据水的作用分析;
(2)根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度的大小,②查出某物质在某温度下的溶解度,从而确定一定量的溶剂中最多能溶解的溶质的多少,从而计算出饱和溶液中溶质的质量分数,③判断物质的溶解度随温度变化的变化情况等.
(3)运用溶解度受温度影响大的降低温度就会有大量的晶体析出、溶解度受温度影响小的就不会大量析出和溶解度的概念解答.
(2)根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度的大小,②查出某物质在某温度下的溶解度,从而确定一定量的溶剂中最多能溶解的溶质的多少,从而计算出饱和溶液中溶质的质量分数,③判断物质的溶解度随温度变化的变化情况等.
(3)运用溶解度受温度影响大的降低温度就会有大量的晶体析出、溶解度受温度影响小的就不会大量析出和溶解度的概念解答.
解答:解:(1)A、配制0.9%的生理盐水时,水作为溶剂,
B、生石灰变成熟石灰,水与氧化钙反应,作为氧化物,
C、浓硫酸稀释时,水作为溶剂,
(2)①根据两物质的溶解度曲线不难看出,溶解度受温度影响较小的是NaCl;根据两物质的溶解度曲线可知,在t1℃时,两物质的溶解度的大小关系是氯化钠>硝酸钾;
②由于在t2℃时,硝酸钾的溶解度是50g,即在100g水中最多溶解25g硝酸钾,则在50g水中最多溶解12.5g硝酸钾,则所得溶液中溶质的质量分数为:
×100%=20%.
(3)硝酸钾的溶解度受温度影响大,降低温度就会有大量的晶体析出,氯化钠的溶解度受温度影响小,降温后不会大量析出;室温约是20℃,这时溶液中含有硝酸钾和氯化钠并且都达到饱和.
故答案为:((6分),每空各1分)
(1)AC (2)①NaCl;>②饱和;20% (3)AB
B、生石灰变成熟石灰,水与氧化钙反应,作为氧化物,
C、浓硫酸稀释时,水作为溶剂,
(2)①根据两物质的溶解度曲线不难看出,溶解度受温度影响较小的是NaCl;根据两物质的溶解度曲线可知,在t1℃时,两物质的溶解度的大小关系是氯化钠>硝酸钾;
②由于在t2℃时,硝酸钾的溶解度是50g,即在100g水中最多溶解25g硝酸钾,则在50g水中最多溶解12.5g硝酸钾,则所得溶液中溶质的质量分数为:
| 12.5g |
| 50g+12.5g |
(3)硝酸钾的溶解度受温度影响大,降低温度就会有大量的晶体析出,氯化钠的溶解度受温度影响小,降温后不会大量析出;室温约是20℃,这时溶液中含有硝酸钾和氯化钠并且都达到饱和.
故答案为:((6分),每空各1分)
(1)AC (2)①NaCl;>②饱和;20% (3)AB
点评:本题考查溶解度的概念、固体的溶解度曲线、固体物质溶解度与温度的关系和溶质质量分数的相关知识,注重知识应用、计算和识图能力的综合考查.

练习册系列答案
相关题目
锡(Sn)是五金之一,它的金属活动性顺序位于铁和铜之间,则下列反应不会发生的是( )
| A、Sn+MgSO4=SnSO4+Mg |
| B、Sn+2HCl═SnCl2+H2↑ |
| C、Sn+2AgNO3=Sn(NO3)2+2Ag |
| D、Zn+Sn(NO3)2=Zn(NO3)2+Sn |

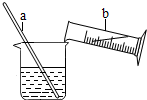 如图是稀释浓硫酸的实验示意图.
如图是稀释浓硫酸的实验示意图.