题目内容
19.下列说法正确的是( )| A. | 同一种元素在同一化合物里的化合价不一定相同 | |
| B. | Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | |
| C. | Al2($\stackrel{-2}{S{O}_{4}}$)3中化学式上方的“2”表示3个硫酸根的化合价为-2价 | |
| D. | 在KMnO4和CaMnO4两种物质中画线部分属于不同种原子团 |
分析 A、根据常见物质中元素的化合价进行分析.
B、标在元素符号右上角的数字表示离子所带电荷数.
C、根据化合价表示方法进行分析.
D、根据原子团的区分进行分析判断.
解答 解:A、同一种元素在同一化合物里的化合价不一定相同,例如硝酸铵中氮元素显-3、+5,故选项说法正确.
B、标在元素符号右上角的数字表示离子所带电荷数,Fe2+中的“2”表示一个亚铁离子带有两个单位的正电荷,故选项说法正确.
C、化学式上方的“2”表示硫酸根的化合价为-2价,故选项说法错误.
D、高锰酸钾中的原子团是高锰酸根,锰酸钙中的原子团是锰酸根,故选项说法正确.
故选:ABD.
点评 本题难度不大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.铁在生产生活中应用十分广泛.铁的冶炼和利用已成为目前科学研究和技术领域中的重要课题.
一、生活中使用的防寒热贴利用了铁生锈原理,其工作过程中实现了由化学能转化为热能.
二、铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来,得到铁合金.一氧化碳还原氧化铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)甲同学为探究铁合金中铁的质量分数,先后进行了四次实验(杂质不与稀硫酸反应),实验数据如表:
请回答:上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则Y=0.9 g,该铁合金中铁的质量分数是多少(写出计算过程)?
(2)乙同学提出单质碳也具有还原性,碳还原氧化铁的化学方程式为2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,为什么工业上不用焦炭作为还原剂直接还原铁矿石?于是,他模拟工业炼铁设计如下对比实验(查阅资料获知NaOH溶液可吸收CO2气体):
①取两份相同质量的氧化铁粉末.一份与足量的碳粉均匀混合放入如图装置A的硬质试管中;另一份放入如图装置B的硬质玻璃管中.

②装置A和B两组实验同时开始进行.在装置B的反应中,实验开始前,先通CO (选填“通CO“或“加热“);实验结束后,继续通入C0直至冷却至室温.
此时,发现装置B的硬质玻璃管中固体完全由红色变为黑色,装置A的硬质试管中仍有红色固体.因而他认为焦炭和铁矿石都是固体,接触面积小,不易完全反应是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因.
(3)丙同学经过查阅资料发现除了上述原因外,工业上不用焦炭作为还原剂直接还原铁矿石还有一些其它原因,试写出其中的一个生铁和焦炭都是固体,不易分离.
(4)丁同学利用图B装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
从上表可以看出进行第2次实验时,所得数据十分不可靠,故舍去.请分析造成此种结果的原因主要可能是反应时间太短.
一、生活中使用的防寒热贴利用了铁生锈原理,其工作过程中实现了由化学能转化为热能.
二、铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来,得到铁合金.一氧化碳还原氧化铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)甲同学为探究铁合金中铁的质量分数,先后进行了四次实验(杂质不与稀硫酸反应),实验数据如表:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量∕g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
| 生成氢气的质量∕g | 0.3 | 0.3 | 0.3 | Y |
(2)乙同学提出单质碳也具有还原性,碳还原氧化铁的化学方程式为2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,为什么工业上不用焦炭作为还原剂直接还原铁矿石?于是,他模拟工业炼铁设计如下对比实验(查阅资料获知NaOH溶液可吸收CO2气体):
①取两份相同质量的氧化铁粉末.一份与足量的碳粉均匀混合放入如图装置A的硬质试管中;另一份放入如图装置B的硬质玻璃管中.

②装置A和B两组实验同时开始进行.在装置B的反应中,实验开始前,先通CO (选填“通CO“或“加热“);实验结束后,继续通入C0直至冷却至室温.
此时,发现装置B的硬质玻璃管中固体完全由红色变为黑色,装置A的硬质试管中仍有红色固体.因而他认为焦炭和铁矿石都是固体,接触面积小,不易完全反应是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因.
(3)丙同学经过查阅资料发现除了上述原因外,工业上不用焦炭作为还原剂直接还原铁矿石还有一些其它原因,试写出其中的一个生铁和焦炭都是固体,不易分离.
(4)丁同学利用图B装置,取不同质量的铁的氧化物进行实验.所得实验数据如下:
| 实验序号 | 铁的氧化物质量/g | 生成铁的质量/g |
| 1 | 4.00 | 2.81 |
| 2 | 8.00 | 7.62 |
| 3 | 10.00 | 7.01 |
| 4 | 12.00 | 8.42 |
| 5 | 14.00 | 9.81 |
| 6 | 16.00 | 11.22 |
| 7 | 18.00 | 12.63 |
| 8 | 20.00 | 14.03 |
4.为测定某纯碱样品中碳酸钠的质量分数(仅含少量NaCl),准确称量W0g样品进行实验,下列实验方案和测量数据最合理(除W0外)的是( )
| 选项 | 实验方法 | 实验方案 | 测量数据 |
| A | 重量法 | 将样品配成溶液,加入过量的硝酸银溶液,过滤 | 得到的沉淀质量 |
| B | 重量法 | 将样品与盐酸反应,生成的气体用浓硫酸吸收 | 浓硫酸增重 |
| C | 重量法 | 将样品放入烧瓶中,置于电子天平上,加入足量浓盐酸 | 减轻的质量 |
| D | 量气法 | 将样品与盐酸反应,气体通过排水量气装置量气 | 排水体积 |
| A. | A | B. | B | C. | C | D. | D |
11.下列操作正确的是( )
| A. | 用酒精灯加热试管里的液体时,试管里的液体不应超过试管容积的$\frac{2}{3}$ | |
| B. | 实验后剩余的药品应放回原试剂瓶中,避免浪费 | |
| C. | 洗过的玻璃仪器内壁附着的水滴既不聚成水滴,也不成股流下时,表明仪器已洗干净 | |
| D. | 不小心碰倒酒精灯,洒出的酒精在桌上燃烧起来时,应立即用水扑灭 |
8.下列物质即可用酚酞溶液,又可以用紫色石蕊溶液鉴别的是( )
| A. | 氢氧化钙溶液和氢氧化钠溶液 | B. | 稀盐酸和氨水 | ||
| C. | 氯化钠液和稀盐酸 | D. | 硝酸钾溶液和水 |
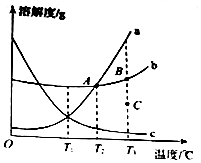 观察图a、b、c三种固体物质的溶解度曲线,探究下列问题:
观察图a、b、c三种固体物质的溶解度曲线,探究下列问题: