题目内容
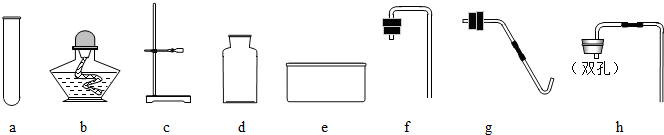
实验室用加热高锰酸钾来制取氧气.经探究:实验生成氧气的质量约是高锰酸钾质量的十分之一.(1)现有高锰酸钾32克,最多能生成氧气多少克?
(2)这些氧气体积为多少升?(空气的密度为1.429g/L)(保留一位小数)
【答案】分析:(1)根据题目是的已知信息“经探究,生成氧气的质量约是高锰酸钾质量的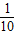 .”可由高锰酸钾的质量求出大约生成氧气的质量;
.”可由高锰酸钾的质量求出大约生成氧气的质量;
(2)根据(1)中求出的氧气质量,利用公式:m=ρv的推导公式v=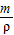 求出氧气的体积即可.
求出氧气的体积即可.
解答:解:(1)∵生成氧气的质量约是高锰酸钾质量的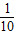 ,
,
∴氧气的质量:32g×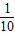 =3.2g;
=3.2g;
(2)由公式m=ρv的推导公式v=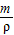 ρ可求出氧气的体积.
ρ可求出氧气的体积.
∴氧气的体积: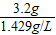 ≈2.2L
≈2.2L
答:(1)大约能生成氧气的质量是3.2g;(2)这些氧气体积为2.2L;
点评:本题立意较简单,只要掌握简单的计算方法和体积质量密度三者之间的公式换算关系即解,需要指出的是根据题意来求生成氧气的质量,而非根据化学方程式来求解;
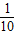 .”可由高锰酸钾的质量求出大约生成氧气的质量;
.”可由高锰酸钾的质量求出大约生成氧气的质量;(2)根据(1)中求出的氧气质量,利用公式:m=ρv的推导公式v=
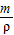 求出氧气的体积即可.
求出氧气的体积即可.解答:解:(1)∵生成氧气的质量约是高锰酸钾质量的
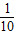 ,
,∴氧气的质量:32g×
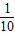 =3.2g;
=3.2g;(2)由公式m=ρv的推导公式v=
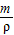 ρ可求出氧气的体积.
ρ可求出氧气的体积.∴氧气的体积:
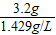 ≈2.2L
≈2.2L答:(1)大约能生成氧气的质量是3.2g;(2)这些氧气体积为2.2L;
点评:本题立意较简单,只要掌握简单的计算方法和体积质量密度三者之间的公式换算关系即解,需要指出的是根据题意来求生成氧气的质量,而非根据化学方程式来求解;

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目