题目内容
实验室要配制100g溶质质量分数为10%的氯化钠溶液。
(1)需氯化钠的质量为_____g;配制时应选择_____(选填“10”“50”或“100”)mL的量筒量取所需水的体积。
(2)某同学按如图所示步骤依次操作:

以上操作中会导致氯化钠溶液的溶质质量分数偏低的步骤是_____(填字母序号)。
(3)操作E中用玻璃棒搅拌,其目的是_____。
(4)若改用20%的氯化钠溶液和水配制上述溶液,需要20%的氯化钠溶液质量是_____g。
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案学习合金知识后,知道了不锈钢中含有金属铬。某同学想:铬与常见铁、铜相比,其金属活动性强弱如何呢?于是,和同学们一起进行了以下探究。
(查阅资料)①铬是银白色有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜:②能与稀硫酸反应,生成硫酸亚铬(CrSO4)。
(知识回顾)金属活动性顺序: K Ca Na Mg Al Zn_______Sn Pb(H)_______Hg Ag Pt Au(在横线上填写对应金属的元素符号)
(作出猜想)猜想①Cr>Fe>Cu;猜想②Fe>Cu>Cr;猜想③__________________。
(设计与实验)①张明同学取大小相等的铁、铜、铬三种金属片,未经打磨就分别放入等量等浓度的稀硫酸中,记录如下:
t度实验操作 | 铁片放在稀硫酸酸中 | 铜片放在稀硫酸中 | 铬片放在稀硫酸中 |
开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 |
结论 | 金属活动性强弱:Fe>Cu,Fe>Cr |
②李红同学也取大小相等的铁、铜、铬三种金属片,先用砂纸打磨后再分别放人等量等浓度的稀硫酸中,记录如下:
实验操作 | 铁片放在稀硫酸中呈黄色。 | 铜片放在稀硫酸中折 | 铬片放在稀硫酸中 |
开始的现象 | 产生少量气泡 | 无气泡 | 产生大量气泡 |
结论 | 金属活动性强弱:_____ >_____ > ____ (填元素符号) |
(讨论交流)为什么张明和李红两个同学记录的铬与稀硫酸反应开始的现象截然不同?
原因是__________________________________________________。
(实验验证)为了进一步确认铁、铜、铬三种金属的活动性强弱,刘斌同学将打磨过的两块铁片分别放人硫酸亚铬(CrSO4)溶液和硫酸铜溶液中,观察到在硫酸亚铬溶液中无明显现象,而在硫酸铜溶液中有明显的现象是__________________________________________,其反应的化学方程式是__________________________________________________。
(拓展迁移)写出铬与稀硫酸反应,生成CrSO4的化学反应方程式____________________。
下列对溶液中溶质和溶剂的判断正确的是_____
选项 | 溶液 | 溶质 | 溶剂 |
A | 硫酸铜溶液 | 铜 | 硫酸 |
B | 医用酒精 | 水 | 酒精 |
C | 稀盐酸 | 氯化氢 | 水 |
D | 碘酒 | 碘 | _____ |
如图所示,将液体X加入到集气瓶中与固体Y作用,观察到气球逐渐变大,如表中液体X和固体Y的组合,符合题意的是( )
① | ② | ③ | ④ | ⑤ | |
X | 稀盐酸 | 水 | 水 | 双氧水 | 水 |
Y | 铁粉 | 氢氧化钠 | 氯化钠 | 二氧化锰 | 硝酸铵 |

A. ①②⑤ B. ①③④ C. ①②④ D. ②③⑤


 干冰用于血液制品的运输 B.
干冰用于血液制品的运输 B.  石墨做电极
石墨做电极 钛合金制造人造骨 D.
钛合金制造人造骨 D.  碳酸钙做人民大会堂的柱子
碳酸钙做人民大会堂的柱子 B.
B. 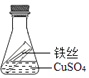
 D.
D. 
 B.
B. 
 D.
D.