题目内容
8.新闻资料:我国于2007年10月24日“嫦娥一号”的成功发射是我国迈出地球的第一步,是中国航天事业发展的又一重大里程碑.月球作为地球的卫星被专家视为地球的“后院”和“第八大洲”,有着可以为人类利用的丰富资源.现有科学探索发现,月球上蕴藏着丰富的钛、铁、铀、钍、稀土、镁、磷、硅、钠、钾、镍、铬、锰等矿产,其中钛铁矿(FeTiOx),不仅是生产金属铁、钛的原料,这所含的氧还是未来月球基地生活用水和生产用水的重要来源.月球的土壤和岩石中蕴藏着丰富的“氦-3”燃料,“氦-3”是一种高效、清洁、安全、廉价的核聚变发电燃料.在地球矿产资源面临耗尽、石油枯竭迟早到来的情况下,载人航天登上月球,可以使之成为人类探测宇宙的前哨,对解决人类持续发展即将面临的难题具有重大意义.根据以上信息回答下列问题:
(1)月球上蕴藏着丰富的钛、铁、铀、钍、稀土、镁、磷、硅、钠、钾、镍、铬、锰等矿产,这里的钛、铁、铀、…,指的是元素(选填“单质”“元素”“原子”).
(2)月岩中钛铁矿主要成分的化学式为FeTiOx,其中铁元素和钛元素的化合价均显+3价.则
x为3.
(3)发射“嫦娥一号”的长三甲火箭燃料是偏二甲肼(X),氧化剂是四氧化二氮(N2O4),燃烧的化学方程式为:X+2N2O4 ═3N2+2CO2+4H2O,X的化学式为C2N2H8.
(4)“嫦娥一号”所用的燃料是液态氢,助燃剂是液态氧,燃烧时产生巨大和推动力将“嫦娥”送上了太空.
①写出氢气燃烧的反应化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
②液态氢作燃料除了燃烧时产生较大的推动力外,另一个优点是产物无污染.
分析 (1)矿物质中的“钛、铁、铀、…”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据在化合物中正负化合价代数和为零,结合钛铁矿主要成分的化学式进行解答本题.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
(4)①氢气燃烧生成水,写出反应的化学方程式即可.
②液态氢作燃料,燃烧产物是水,据此进行分析解答.
解答 解:(1)矿物质中的“钛、铁、铀、…”等不是以单质、分子、原子等形式存在,这里所指的“钙、锌、碘”是强调存在的元素,与具体形态无关.
(2)钛铁矿主要成分的化学式为FeTiOx,其中铁元素和钛元素的化合价均显+3价,氧元素显-2价,则(+3)+(+3)+(-2)×x=0,x=3.
(3)根据反应的化学方程式X+2N2O4═3N2+2CO2+4H2O,反应物中氮、氧原子个数分别为4、8,反应后的生成物中氮、碳、氢、氧原子个数分别为6、2、8、8,根据反应前后原子种类、数目不变,则每个X分子由2个碳原子、2个氮原子和8个氢原子构成,则物质X的化学式为C2N2H8.
(4)①氢气燃烧生成水,反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
②液态氢作燃料,燃烧产物是水,无污染.
故答案为:(1)元素;
(2)3;(3)C2N2H8;
(4)①2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;②产物无污染.
点评 本题难度不大,掌握元素的概念、利用化合价的原则计算指定元素的化合价的方法、质量守恒定律、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.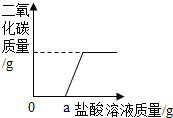
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
计算该样品中Na2CO3的质量分数(写出计算过程).
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示. 请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).

(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示. 请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
16.下列各组物质的鉴别方法不正确的是( )
| 选项 | 物质 | 鉴别方法 |
| A | 氧化铜粉末和铁粉 | 用磁铁吸引 |
| B | 氢氧化钠和硝酸铵 | 加水后测温度变化 |
| C | 氯化铵和硫酸铵 | 加入熟石灰粉末研磨 |
| D | 羊毛纤维和合成纤维 | 点燃后闻气味 |
| A. | A | B. | B | C. | C | D. | D |
13.在CuCl2和ZnCl2的混合液中加过量的铁粉,充分反应后过滤,留在滤纸上的物质是( )
| A. | Cu | B. | Fe | C. | Cu和Zn | D. | Cu和Fe |
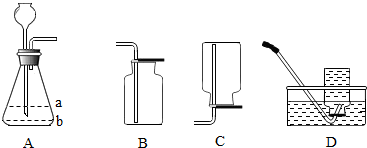
4. 为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
 为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )
为验证混合气体中是否含有CO,CO2,H2O,H2 这四种气体,现有无水硫酸铜,澄清石灰水,浓硫酸,氢氧化钠溶液以及如图所示装置甲.能验证这四种气体的方法正确的是( )| A. | 依次通入无水硫酸铜,澄清石灰水,浓硫酸,甲装置,无水硫酸铜,澄清石灰水 | |
| B. | 依次通入无水硫酸铜,澄清石灰水,甲装置,无水硫酸铜,澄清石灰水 | |
| C. | 依次通入澄清石灰水,无水硫酸铜,浓硫酸,甲装置,无水硫酸铜,澄清石灰水 | |
| D. | 依次通入无水硫酸铜,澄清石灰水,浓硫酸,甲装置,澄清石灰水,无水硫酸铜 |