题目内容
12.根据下列图回答: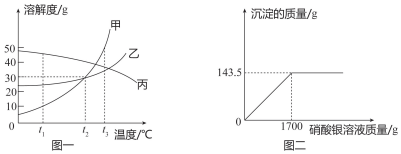
(1)图一表示甲、乙、丙三种物质的溶解度曲线.
①t2℃时,甲、乙的溶解度均为30g.
②t1℃时,饱和丙溶液升高温度,观察的现象是溶液变浑浊.
③将甲、乙、丙三种物质t1℃时的饱和溶液升高到t3℃,所得溶液中溶质的质量分数从大到小关系是丙>乙>甲.
(2)某学习小组用模拟海水测定其中氯元素的质量分数.取模拟海水(含NaCl、MgCl2)2000g,向溶液中滴加10%的硝酸银溶液,其沉淀质量变化如图二.
①沉淀的化学式为AgCl
②模拟海水中氯的质量分数是1.8%(结果保留一位小数)
分析 (1)根据物质的溶解度曲线可以判断相关方面的问题;
(2)银离子和氯离子结合生成白色沉淀氯化银,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)①t2℃时,甲、乙的溶解度均为30g.
故填:30g.
②丙的溶解度随着温度升高而减小,t1℃时,饱和丙溶液升高温度时析出固体,观察到溶液变浑浊.
故填:溶液变浑浊.
③t1℃时乙的溶解度大于甲,因此乙的饱和溶液质量分数大于甲的饱和溶液质量分数,温度升高到t3℃时,都变成不饱和溶液,都是质量分数都不变,因此乙的质量分数大于甲,因为t3℃时丙的溶解度大于t1℃时甲、乙的溶解度,温度升高到t3℃时,丙的质量分数大于甲、乙的质量分数,因此将甲、乙、丙三种物质t1℃时的饱和溶液升高到t3℃,所得溶液中溶质的质量分数从大到小关系是丙>乙>甲.
故填:丙>乙>甲.
(2)设模拟海水中氯的质量为x,
由NaCl+AgNO3═AgCl↓+NaNO3,MgCl2+2AgNO3═2AgCl↓+Mg(NO3)2可知,Cl~AgCl,
Cl~AgCl,
35.5 143.5
x 143.5g
$\frac{35.5}{x}$=$\frac{143.5}{143.5g}$,
x=35.5g,
模拟海水中氯的质量分数是:$\frac{35.5g}{2000g}$×100%=1.8%,
故填:AgCl;1.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
20.兴趣小组同学发现实验台上整齐摆放的药品中(如图),有一试剂瓶的标签破损.
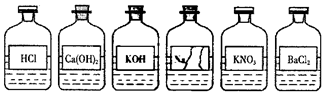
【提出问题】这瓶试剂的成分是什么?
(1)【讨 论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是A;
A.酸 B.碱 C.盐
【猜 想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl(任写一种).
(2)【设计并实验】
(3)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择上图已有的一种试剂就能把它鉴别出来.他们又进行了实验.

【提出问题】这瓶试剂的成分是什么?
(1)【讨 论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是A;
A.酸 B.碱 C.盐
【猜 想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl(任写一种).
(2)【设计并实验】
(3)小明认为它是NaOH溶液,小俊认为它是Na2CO3溶液.要进一步确定它的成分,小俊认为只需选择上图已有的一种试剂就能把它鉴别出来.他们又进行了实验.
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中 | 猜想②正确 相关的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑ (或Na2CO3+BaCl2=BaCO3↓+2NaCl) |
4.浓盐酸敞口放置一段时间后,下列关于浓盐酸溶液pH变化的说法正确的是( )
| A. | 变大 | B. | 变小 | C. | 不变 | D. | 无法确定 |
1.如图表示的是一些物质在常温下的近似pH.下列有关这些物质的说法中,正确的是( )

| A. | 苹果汁的酸性大于酸雨的酸性 | |
| B. | 小苏打水不能使酚酞液变红 | |
| C. | 厨房清洁剂的碱性小于小苏打水的碱性 | |
| D. | 酸雨呈酸性的主要原因是溶有二氧化碳 |