题目内容
12.对溶质的质量分数是10%的NaCl溶液含义的解释错误的是( )| A. | 100g水中溶解了10g NaCl | B. | 每100g NaCl溶液中含有10g NaCl | ||
| C. | NaCl与溶液质量之比是1:10 | D. | 将10g NaCl溶于90g水中所得溶液 |
分析 溶液中溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%,溶质的质量分数为10%的溶液即溶液中溶质和溶液的质量之比是1:10,或溶质和溶剂的质量之比为1:9,或溶剂和溶液的质量之比为9:10.
解答 解:溶质的质量分数为10%的溶液即溶液中溶质和溶液的质量之比是1:10,或溶质和溶剂的质量之比为1:9,或溶剂和溶液的质量之比为9:10.
A、10%的食盐溶液即溶液中溶质和溶剂的质量之比为1:9,选项中食盐与水质量之比等于1:9,选项中质量之比溶质和溶液10:100=1:10,故选项含义错误.
B、10%的食盐溶液即溶液中溶质和溶液的质量之比为1:10,选项中质量之比溶质和溶液10:100=1:10,故选项含义正确.
C、10%的食盐溶液即溶液中溶质和溶液的质量之比为1:10,选项中质量之比溶质和溶液1:10,故选项含义正确.
D、10%的食盐溶液即溶液中溶质和溶剂的质量之比为1:9,选项中溶质和溶剂质量之比10:90=1:9,故选项中含义正确.
答案:A
点评 本题难度不大,掌握溶液中溶质的质量分数的概念并能灵活运用即可正确解答本题.

练习册系列答案
相关题目
20.红枣常食有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”.其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】①铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
②碳酸钠溶液和氢氧化钙溶液反应会生成碳酸钙沉淀,反应的方程式为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙会和水反应生成氢氧化钙.
(2)甲同学的实验中如果含有Fe2O3,则会和盐酸发生反应,Fe2O3和盐酸发生反应的方程式为①Fe2O3+6HCl═2FeCl3+3H2O,丙同学思考后认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是②氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色
他们设计如下实验方案继续验证.

乙同学对滤渣B进行探究.
【反思与评价】
(1)乙同学经过实验测得上述滤渣C的质量为1.0g,计算滤液A中含氢氧化钙的质量.(写出解题过程)
(2)丙同学经过实验测得磁铁吸引后残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g.综合上述实验及乙、丙同学的数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
(3)结合固体的成分,你认为这包“504双吸剂”,除了能吸收空气中的水分外,还能吸收空气中的氧气从而达到防腐的作用.
【提出问题】久置固体的成分是什么?
【查阅资料】①铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
②碳酸钠溶液和氢氧化钙溶液反应会生成碳酸钙沉淀,反应的方程式为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有①CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量②气泡产生,得到浅绿色溶液. | 固体中一定含有③Fe, 一定不含Fe2O3 |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙会和水反应生成氢氧化钙.
(2)甲同学的实验中如果含有Fe2O3,则会和盐酸发生反应,Fe2O3和盐酸发生反应的方程式为①Fe2O3+6HCl═2FeCl3+3H2O,丙同学思考后认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是②氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色
他们设计如下实验方案继续验证.

乙同学对滤渣B进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡冒出、溶液变为黄色溶液变为黄色、澄清的石灰水变浑浊 澄清的石灰水变浑浊 | 固体中一定含有 ③CaCO3和Fe2O3 |
(1)乙同学经过实验测得上述滤渣C的质量为1.0g,计算滤液A中含氢氧化钙的质量.(写出解题过程)
(2)丙同学经过实验测得磁铁吸引后残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g.综合上述实验及乙、丙同学的数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
(3)结合固体的成分,你认为这包“504双吸剂”,除了能吸收空气中的水分外,还能吸收空气中的氧气从而达到防腐的作用.
7.某同学梳理归纳了以下知识点:①用水灭火的原理是降低了可燃物的着火点;②打开浓盐酸的瓶盖瓶口冒白烟;③用pH试纸测液体的pH只能是整数;④防毒面具的原理是利用活性炭的吸附性;⑤洗涤剂能去除油污是因为洗涤剂可以溶解油污;⑥用氢氧化钠溶液来制作“叶脉书签”,是因为氢氧化钠有腐蚀性.其中正确的组合是( )
| A. | ①⑤⑥ | B. | ②④⑤ | C. | ③⑤⑥ | D. | ③④⑥ |
17.欲配制25g质量分数为10%的氯化钠溶液,下列说法不正确的是( )
| A. | 实验中用到的玻璃仪器只有烧杯和量筒 | |
| B. | 计算得氯化钠的质量为2.5g,水的体积为22.5ml | |
| C. | 量取水时,若俯视读数,会使配得的溶液浓度偏大 | |
| D. | 用天平称取该固体时将砝码和物品放反,会导致配得的溶液浓度偏小 |
4.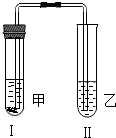 按如图所示装置进行实验(图中铁架台等仪器均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台等仪器均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
 按如图所示装置进行实验(图中铁架台等仪器均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台等仪器均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )| A. | 甲:NaHCO3、稀HCl 乙:NaOH | |
| B. | 甲:Al、稀H2SO4 乙:Ba(NO3)2溶液 | |
| C. | 甲:MgO、稀盐酸 乙:AgNO3 | |
| D. | 甲:Cu、稀H2SO4 乙:BaCl2溶液 |
2.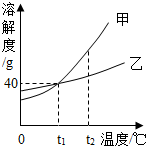 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法错误的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法错误的是( )
 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法错误的是( )
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法错误的是( )| A. | t2℃时,甲物质的溶解度大于乙物质的溶解度 | |
| B. | t1℃时,甲、乙两种物质各50g分别加入到100g水中,充分溶解,得到的溶液质量都是140g | |
| C. | t1℃时,甲、乙两种物质的溶液的溶质质量分数一定相等 | |
| D. | t2℃时等质量的甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙 |
 “高钙片”是一种常见补钙剂,如图是“高钙片”说明书的一部分.
“高钙片”是一种常见补钙剂,如图是“高钙片”说明书的一部分.