题目内容
6.下列物质中属于碱的是( )| A. | K2CO3 | B. | NH3•H2O | C. | C2H5OH | D. | Cu2(OH)2CO3 |
分析 碱是指在电离时产生的阴离子全部是氢氧根离子的化合物,据此进行分析判断.
解答 解:A、K2CO3是由钾离子和碳酸根离子构成的化合物,属于盐,故选项错误.
B、NH3•H2O是由铵根离子和氢氧根离子构成的化合物,属于碱,故选项正确.
C、C2H5OH是含碳元素的化合物,属于有机物,故选项错误.
D、Cu2(OH)2CO3是由铜离子、氢氧根离子、碳酸根离子构成的化合物,含有金属离子和酸根离子,属于盐,故选项错误.
故选:B.
点评 本题难度不大,考查物质类别的判别,抓住酸、碱、盐的特征、熟悉常见的物质的组成是正确解答本题的关键.

练习册系列答案
相关题目
17.《火锅英雄》的上映让全国人民再一次加深了对重庆的印象.下列做法有利于提升重庆火锅名誉的是( )
| A. | 用霉变花生榨汁 | B. | 用甲醛保鲜鹅肠 | ||
| C. | 用陶瓷碗代替一次性塑料碗 | D. | 用工业盐亚硝酸钠调味 |
14.下列图示实验操作中,正确的是( )
| A. |  | B. | 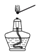 | C. |  | D. | 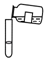 |
1.下列有关构成物质的粒子的说法正确的是( )
| A. | 一种原子只能构成一种分子 | |
| B. | 质子数相等的粒子一定属于同种元素 | |
| C. | 原子得失电子形成离子时,其电子层数可能有变化 | |
| D. | 同种元素的粒子,其核外电子数一定相同 |
11.下列说法不符合客观事实的是( )
| A. | 生活中,氯化钠做融雪剂 | B. | 医疗上,碳酸钙做补钙剂 | ||
| C. | 工业上,纯碱用于制玻璃 | D. | 测pH时,将pH试纸浸入农夫山泉中 |
18.夏天晾衣服比冬天干得快,从这一生活经验不能得出的结论是( )
| A. | 水分子很小 | B. | 温度较高时水分子的运动加快 | ||
| C. | 水分子是不断运动的 | D. | 水分子化学性质发生了改变 |
3.对比分析是化学研究和学习的基本方法.甲、乙、丙三位同学利用图中的装置,围绕“用称量的方法验证化学反应是否遵守质量守恒定律并分析实验条件”这一探究目的开展活动.

【实验步骤】
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在两个托盘天平上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别利用装置进行化学反应.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
(2)比较甲、丙同学的实验有许多相似之处,如生成物都属于氧化物(填物质的类别).
(3)通过对上述实验的对比分析,甲、乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有反应前未称量参加反应的氧气质量,反应后部分生成的氧化镁扩散到空气中,无法称量.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】(4)请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.

【实验步骤】
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在两个托盘天平上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别利用装置进行化学反应.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | 化学方程式 | 结 论 | |
| 甲同学 | 白磷燃烧产生大量白烟,放热、气球先膨胀,后变小、天平平衡 | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 该反应遵守质量守恒定律 |
| 乙同学 | 烧杯中有大量气泡产生、天平不平衡 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | 该反应遵守质量守恒定律 |
| 丙同学 | 镁条剧烈燃烧,发出耀眼白光,放热,生成白色固体.反应前后称量质量不相等 | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 该反应不遵守质量守恒定律 |
(3)通过对上述实验的对比分析,甲、乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有反应前未称量参加反应的氧气质量,反应后部分生成的氧化镁扩散到空气中,无法称量.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】(4)请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
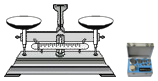
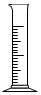
 为测定一标签破损(如图)的钙片中碳酸钙的含量,某同学做如下实验:取5片钙片,放入干燥、洁净的烧杯中,然后逐滴滴加稀盐酸,当加入30g盐酸后,恰好完全反应,此时称量烧杯内剩余物质的总质量为37.8g.(钙片中其他成分不和稀盐酸反应,反应中产生的气体全部放出)
为测定一标签破损(如图)的钙片中碳酸钙的含量,某同学做如下实验:取5片钙片,放入干燥、洁净的烧杯中,然后逐滴滴加稀盐酸,当加入30g盐酸后,恰好完全反应,此时称量烧杯内剩余物质的总质量为37.8g.(钙片中其他成分不和稀盐酸反应,反应中产生的气体全部放出)