题目内容
人体缺少钙元素会影响健康,因此每日需摄人足够的钙.维生素D能促进钙的吸收,维生素D种类很多,其中维生素D2的化学式为C28H44O.如图是某钙制剂的部分说明,某兴趣小组欲检验“每片含钙500mg”的真伪,进行了如下实验:

①取2片钙片研碎;②将其加入足量稀盐酸中充分反应;③收集到1.1gCO2.试计算:
(1)维生素D2的相对分子质量为 ;维生素D2中碳、氢元素的质量比为 ;碳酸钙中钙的质量分数为 .
(2)帮助兴趣小组的同学计算判断此钙剂中钙含量与标注是否属实.(假设钙片中其他成分不与稀盐酸反应)

①取2片钙片研碎;②将其加入足量稀盐酸中充分反应;③收集到1.1gCO2.试计算:
(1)维生素D2的相对分子质量为
(2)帮助兴趣小组的同学计算判断此钙剂中钙含量与标注是否属实.(假设钙片中其他成分不与稀盐酸反应)
考点:标签上标示的物质成分及其含量,相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:标签图示型
分析:(1)根据化学式进行计算:①D2的相对分子的质量;维生素D2中碳、氢元素的质量比及维生素;根据碳酸钙的化学式进行计算碳酸钙(CaCO3)中钙元素的质量分数解答;
(2)根据碳酸钙与盐酸反应的方程式,将二氧化碳的质量代入计算可判断碳酸钙的质量,然后乘以钙在碳酸钙中所占有的质量分数,求出钙元素的质量与补钙剂的说明比较判定是否属实.
(2)根据碳酸钙与盐酸反应的方程式,将二氧化碳的质量代入计算可判断碳酸钙的质量,然后乘以钙在碳酸钙中所占有的质量分数,求出钙元素的质量与补钙剂的说明比较判定是否属实.
解答:解:
(1)维生素D2的相对分子质量:12×28+1×44+16=396;维生素D2中碳、氢元素的质量比是:(12×28):(1×44)=84:11;碳酸钙(CaCO3)中钙元素的质量分数为:
×100%=40%;
(2)因盐酸足量,则碳酸钙完全反应;
设片钙片中碳酸钙的质量为x,1片与足量稀盐酸中充分反应,收集到0.55gCO2.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 0.55g
=
解得x=1.25g,
则1.25g碳酸钙中含钙元素的质量为:1.25g×40%=0.5g
0.5g×1000mg/g=500mg
与说明中每片含钙500mg、一致,则说明属实,
答案:
(1)396 84:11 40%
(2)此钙片中钙含量与标注属实.
(1)维生素D2的相对分子质量:12×28+1×44+16=396;维生素D2中碳、氢元素的质量比是:(12×28):(1×44)=84:11;碳酸钙(CaCO3)中钙元素的质量分数为:
| 40 |
| 40+12+16×3 |
(2)因盐酸足量,则碳酸钙完全反应;
设片钙片中碳酸钙的质量为x,1片与足量稀盐酸中充分反应,收集到0.55gCO2.
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 0.55g
| 100 |
| x |
| 44 |
| 0.55g |
解得x=1.25g,
则1.25g碳酸钙中含钙元素的质量为:1.25g×40%=0.5g
0.5g×1000mg/g=500mg
与说明中每片含钙500mg、一致,则说明属实,
答案:
(1)396 84:11 40%
(2)此钙片中钙含量与标注属实.
点评:本题考查利用化学式和化学反应方程式的计算,学生明确常化学式计算的方法、化学反应中何种物质的质量可代入方程式计算是解答的关键.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
空气里各种成分都有它们各自的特性和主要用途,请你根据有关成分的特性和用途,在下表中填空:
| 空气中成分的名称 | 特性 | 用途 |
| 支持呼吸和燃烧 | 供给生物呼吸 | |
| 氮气 | 作保护气、制化肥 | |
| 通电会发紫蓝色的光 | ||
| 密度很小、很稳定 | 填充气球 |
规范实验操作是获得实验成功的重要保证.下列实验中正确的是( )
A、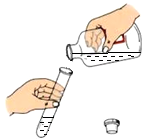 倾倒液体 |
B、 检查气密性 检查气密性 |
C、 过滤 |
D、 闻气味 |
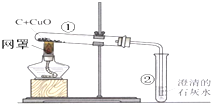 化学课上演示用木炭还原氧化铜的实验如图.
化学课上演示用木炭还原氧化铜的实验如图.