题目内容
14.根据如图1装置图,回答有关问题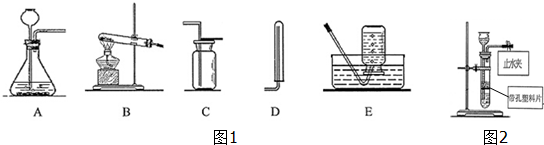
(1)B中用到的两件玻璃仪器的名称试管、酒精灯.
(2)写出用B装置制取氧气的化学方程式2KClO3$\frac{\underline{催化剂}}{△}$2KCl+3O2↑.收集装置可选用C(填序号,一种即可),原因是氧气的密度比空气大且不和空气的成分反应.
(3)若发生装置选A,收集装置选D,则可以制取气体的反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑.
(4)某兴趣小组将B装置改进,如图2所示,请你指出该装置的一个优点:控制反应的发生与停止.
分析 (1)从B中用到的两件玻璃仪器为试管和酒精灯去分析;
(2)由A装置的特点是加热固体制取气体,且试管口没放棉花团,故选用的药品是氯酸钾和二氧化锰;由于氧气不易溶于水,所以可以用排水法收集,由于氧气的密度比空气大且不和空气的成分反应,故可用向上排空气法收集去分析;
(3)从发生装置选A,收集装置选D,由于用向下排空气法收集,故是固体和液体反应制取气体且密度比空气密度小,可知制取的是氢气去分析;
(4)从在图2装置查可控制反应的发生与停止去分析.
解答 解:(1)B中用到的两件玻璃仪器为试管和酒精灯;故答案为:试管 酒精灯;
(2)由于A装置的特点是加热固体制取气体,且试管口没放棉花团,故选用的药品是氯酸钾和二氧化锰;加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气,其化学方程式为:2KClO3$\frac{\underline{催化剂}}{△}$2KCl+3O2↑;由于氧气不易溶于水,所以可以用排水法收集,由于氧气的密度比空气大且不和空气的成分反应,故可用向上排空气法收集;故答案为:2KClO3$\frac{\underline{催化剂}}{△}$2KCl+3O2↑ C(E) 氧气的密度比空气大且不和空气的成分反应(氧气不易溶于水);
(3)若发生装置选A,收集装置选D,由于用向下排空气法收集,故是固体和液体反应制取气体且密度比空气密度小,可知制取的是氢气;实验室可用锌和稀硫酸反应制取氢气;其反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;故答案为:Zn+H2SO4=ZnSO4+H2↑;
(4)在图2装置中,把固体放在隔板上,液体通过长颈漏斗加入,使用时,让液体与固体接触,反应开始,产生气体;不用时,可把导气管用止水夹夹住,产生的气体不能导出试管,造成试管内气体越来越多,压强越来越大,液体被压到长颈漏斗中,固体和液体分离,反应停止.即可以控制反应的发生与停止;故答案为:控制反应的发生与停止.
点评 实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;考查了实验室制取氧气、氢气的反应原理,收集方法等,是考试的重点也是中考的重点.

 百年学典课时学练测系列答案
百年学典课时学练测系列答案是什么催化了过氧化氢反应.
(1)小明猜想是氧化铜催化了过氧化氢反应.
(2)小华猜想是木炭粉催化了过氧化氢反应.
(3)于是二人决定设计实验证明自己的结论.
| 实验操作 | 实验现象 | 实验结论 |
| 取5毫升5%过氧化氢溶液放入试管,将带火星木条伸入试管 | 无气泡产生,木条不复燃 | 过氧化氢溶液本身几乎不反应 |
| 取5毫升5%过氧化氢溶液放入试管,再向试管中加入2克氧化铜,将带火星木条伸入试管.反应完后称量剩余的固体质量. | 有大量气泡产生,木条复燃,反应后称量剩余固体质量为2克. | 氧化铜能催化过氧化氢反应 |
| 取5毫升5%过氧化氢溶液放入试管,再向试管中加入2克木炭粉,将带火星木条伸入试管.反应完后称量剩余的固体质量. | 无气泡产生,木条不复燃.反应后称量剩余固体质量为2克. | 木炭粉不能催化过氧化氢反应. |
| A. | 将空气通过灼热的铜网可以除去氧气 | |
| B. | 用点燃的方法可以除去二氧化碳中的一氧化碳 | |
| C. | pH试纸使用前,先用蒸馏水湿润,再测定未知浓液的pH | |
| D. | 稀释浓硫酸时,向浓硫酸中缓缓加人蒸馏水,用玻璃棒搅拌 |
| A. | Na+、H+、HC03- | B. | Na+、Ca2+、CO32- | C. | K+、N03-、H+ | D. | H+、CI-、OH - |
| A. | 将实验剩余药品放回原试剂瓶 | |
| B. | 过滤时,慢慢地将液体直接倒入过滤器中 | |
| C. | 在溶液蒸发结晶的过程中,当蒸发皿中剩余少量溶液时即停止加热 | |
| D. | 将称量物放在托盘天平右盘上称量 |
| A | B | C | D | |
| 实 验 内 容 |  仪器连接 |  硫的燃烧 | 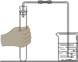 检查气密性 |  准备过滤器 |
| 水 的 作 用 | 连接前用玻璃管端蘸水,起润滑作用. | 瓶中的水起到防止实验时炸裂瓶底的作用. | 形成密闭系统,用于观察现象检查装置是否漏气. | 用胶头滴管滴少量水,让滤纸紧贴漏斗内壁. |
| A. | A | B. | B | C. | C | D. | D |