��Ŀ����
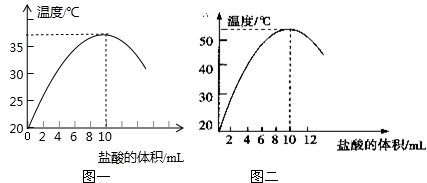
1�����Ͳ�������Fe�۾��й㷺����;��������ͨFe�۸�����������Ӧ�����Ʊ�����������ͼ��ʾ��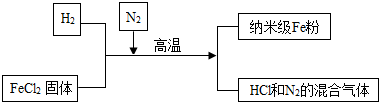
��ش��������⣺
��1������Fe�������������Է�ȼ�����ɺ�ɫ���壬�˺�ɫ����Ļ�ѧʽΪFe3O4��
��2���벹����������Ʊ����յĻ�ѧ����ʽ��H2+FeCl2$\frac{\underline{\;����\;}}{\;}$Fe+2HCl��
��3���о���Ա��������Ƶõ�����Fe����Ʒ�л���������FeCl2���ʣ�
��Ϊ��ȥ��Ʒ�е����ʣ������������£��ȼ�ˮ�ܽ⣬Ȼ���ٹ��ˡ�ϴ�ӡ���ɣ�
��ȡ��Ʒ20g���������������ᣬ��������0.7g����������Ʒ�е���Fe����������������д��������̣�98%��
���� ��1����������������Ӧ�����������������ǣ���2�����ݷ�Ӧǰ�����ԭ���������Ŀ����͵�����ѧ�����ȶ����ǣ���3���ٸ�����������ˮ���Ȼ���������ˮ���л����ķ��룻�ڸ�����������������������������ٳ���20g�������������������
��� �⣺��1������������ȼ���������������������Ժ�ɫ������������������
��2����Ӧ��ķ����к���2����ԭ�ӡ�һ����ԭ�ӡ�2����ԭ�ӣ����������Ѿ�����һ����ԭ�ӣ���ȱ��2����ԭ�Ӻ�2����ԭ�ӣ����Բ����������2HCl��������ѧ�����ȶ����ڷ�Ӧ���𱣻��������ã�
��3������������ˮ���Ȼ���������ˮ�����Լ�ˮ�ܽ⣬�ٽ��й��ˡ�ϴ�Ӹ��T�ɣ�
��������0.7g������Ҫ�μӷ�Ӧ����������ΪX����
Fe+2HCl�TFeCl2+H2��
56 2
X 0.7g
���ݣ�$\frac{56}{2}$=$\frac{x}{0.7g}$���X=19.6g��
$\frac{19.6g}{20g}$��100%=98%
�ʴ�Ϊ����1��Fe3O4����2��2HCl����3����ˮ�����ˣ���������0.7g������Ҫ�μӷ�Ӧ����������ΪX����
Fe+2HCl�TFeCl2+H2��
56 2
X 0.7g
���ݣ�$\frac{56}{2}$=$\frac{x}{0.7g}$���X=19.6g��
$\frac{19.6g}{20g}$��100%=98%��
���� �����ؼ���֪����ȼ�յIJ������������������ܹ�������������غ㶨�ɽ��ʵ�����⣬֪�������Թ����Һ�����ķ�������Ϥ���ݷ���ʽ�ļ��㷽����

 ������ҵ����ν�����������ϵ�д�
������ҵ����ν�����������ϵ�д�| A�� | �������˶�Ь | B�� | ����T�� | ||
| C�� | ����ˮƿ | D�� | ���ڱ��� |

��������ʵ�����������ͬѧ�ó��Ľ��۲���ȷ���ǣ�������
| A�� | ԭ�������һ��û��CuSO4 | |
| B�� | ��ɫ����A�к���BaCO3��BaSO4���ֳ��� | |
| C�� | ��ɫ����Eһ����AgCl���� | |
| D�� | ԭ�������һ����Ba��NO3��2��BaSO4��Na2CO3 |
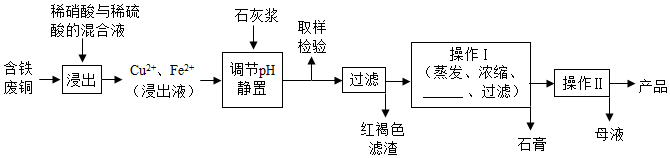
������ʯ���ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ�������
| �¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
| ʯ�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| ���� | 32 | 44.6 | 61.8 | 83.8 | 114 |
��1�����ɫ��������Ҫ�ɷ���Fe��OH��3��
��2�������ķ�ͭ��ϡ���ᷴӦ�Ļ�ѧ����ʽFe+H2SO4=FeSO4+H2����
��3������I����¶�Ӧ�ÿ�����100�����ң�
��4������Һ�з��������ͭ����IJ�����ӦΪ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ������������ˮ�Ҵ���ϴ��Һ����������ˮ��ԭ���Ǽ��������ܽ���ɵ���ʧ��
| ����������Һ������/g | 0 | 2.5 | 3.65 | 6 |
| ��Һ��pH | 12 | 11 | 7 | 2 |
 �����ѧ���������ϴ����Ű��������л�Ĺ�ϵ����ͼ��ʾ�����и�����ϵ˵����ȷ���ǣ�������
�����ѧ���������ϴ����Ű��������л�Ĺ�ϵ����ͼ��ʾ�����и�����ϵ˵����ȷ���ǣ�������| A�� | ���빦�����ڰ�����ϵ | B�� | �������������ڲ��й�ϵ | ||
| C�� | ������ͻ�������ڽ����ϵ | D�� | ����������������ڰ�����ϵ |