题目内容
下表是硝酸钾和氯化铵在不同温度时的溶解度.分析表中数据,回答问题.
(1)上述图1中,甲可表示 的溶解度曲线.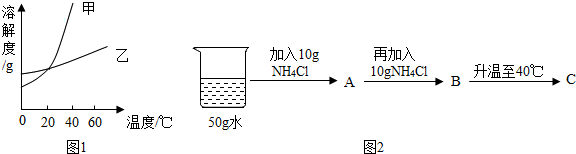
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是 .
(3)20℃时,按图2所示操作:B中的溶液是 (选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为 .
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | |

(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是
(3)20℃时,按图2所示操作:B中的溶液是
考点:固体溶解度曲线及其作用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据物质的溶解度大小可以判断溶解度曲线变化情况,从而可以确定具体的物质;
(2)据饱和溶液中溶质的 质量分数=
×100%可知溶解度打则溶质的质量分数大;
(3)根据20℃时氯化铵的溶解度分析是否是饱和溶液,并可以判断饱和溶液中溶质与溶剂的质量比.
(2)据饱和溶液中溶质的 质量分数=
| 溶解度 |
| 溶解度+100g |
(3)根据20℃时氯化铵的溶解度分析是否是饱和溶液,并可以判断饱和溶液中溶质与溶剂的质量比.
解答:解:(1)由氯化铵和硝酸钾的溶解度可知,硝酸钾的溶解度随温度变化更大,所以图1中能表示KNO3溶解度曲线的是甲;
(2)据饱和溶液中溶质的 质量分数=
×100%可知溶解度大则溶质的质量分数大,60℃时氯化铵的溶解度比硝酸钾的溶解度小,所以两种物质的饱和溶液中,溶质质量分数较小;
(3)20℃时氯化铵的溶解度是37.2g,即100g水中最多溶解37.2g的氯化铵,所以50g水中最多溶解18.6g的溶质,图2中B溶液是50g水中加入了20g的溶质,所以不能完全溶解,得到的是氯化铵的饱和溶液;40℃时氯化铵的溶解度变为45.8g,则50g水中最多溶解溶质的质量大于20g,所以加入的溶质能完全溶解,所得溶液中溶质和溶剂的质量比是20g:50g=2:5;
故答案为:(1)KNO3或硝酸钾;(2)NH4Cl或氯化铵;(3)饱和;2:5.
(2)据饱和溶液中溶质的 质量分数=
| 溶解度 |
| 溶解度+100g |
(3)20℃时氯化铵的溶解度是37.2g,即100g水中最多溶解37.2g的氯化铵,所以50g水中最多溶解18.6g的溶质,图2中B溶液是50g水中加入了20g的溶质,所以不能完全溶解,得到的是氯化铵的饱和溶液;40℃时氯化铵的溶解度变为45.8g,则50g水中最多溶解溶质的质量大于20g,所以加入的溶质能完全溶解,所得溶液中溶质和溶剂的质量比是20g:50g=2:5;
故答案为:(1)KNO3或硝酸钾;(2)NH4Cl或氯化铵;(3)饱和;2:5.
点评:物质的溶解度是物质溶解能力的外在表现,因此要学会观察物质的溶解度曲线,为正确分析相关方面的问题奠定基础.

练习册系列答案
相关题目
下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是( )
| A、闻气味 |
| B、将集气瓶倒扣在水中 |
| C、观察颜色 |
| D、将燃着的木条伸入集气瓶中 |
以下各类盐中,全部可溶于水的是( )
①硫酸盐 ②镁盐 ③硝酸盐 ④碳酸盐 ⑤钠盐 ⑥钾盐.
①硫酸盐 ②镁盐 ③硝酸盐 ④碳酸盐 ⑤钠盐 ⑥钾盐.
| A、⑤和⑥ | B、③⑤和⑥ |
| C、只有③ | D、除去④ |

 如图 是甲、乙两种固体物质的溶解度曲线,回答:
如图 是甲、乙两种固体物质的溶解度曲线,回答:
 2014年3月22日是第二十二届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:
2014年3月22日是第二十二届“世界水日”,水与人类的生活和生产密切相关,请回答下列问题: