题目内容
下列图象不能正确反映其对应变化关系的是( )
|
| A. |
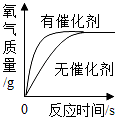
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 |
|
| B. |
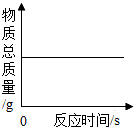
一定质量的红磷在密闭容器中燃烧 |
|
| C. |
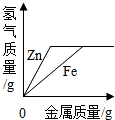
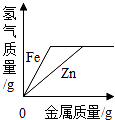
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 |
|
| D. | 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
| 催化剂的特点与催化作用;金属的化学性质;碱的化学性质;质量守恒定律及其应用.. | |
| 专题: | 元素化合物知识型. |
| 分析: | A、根据用等质量、等浓度的双氧水分别制取氧气,有无催化剂只是改变化学反应的速率,不影响生成氧气的量进行解答; B、根据红磷在盛有氧气的密闭集气瓶内燃烧消耗氧气,生成五氧化二磷固体进行解答; C、根据相同质量的情况下铁比锌消耗的硫酸多分析; D、向一定量的盐酸和氯化铜混合溶液中滴加氢氧化钠溶液,先发生中和反应,然后生成Cu(OH)2沉淀. |
| 解答: | 解:A、用等质量、等浓度的双氧水分别制取氧气,有无催化剂只是改变化学反应的速率,不影响生成氧气的量,所以最终生成氧气的质量应该相等,故A正确; B、由质量守恒定律的定义可知,反应前后物质总质量不发生改变,此反应在密闭容器中进行,无其他物质的进入或散失,故物质总质量不会改变,与图象所示吻合,故B正确; C、横坐标表示的不是反应时间,而是金属的质量,产生相同质量的氢气,消耗锌的质量比铁多,故应该是硫酸与铁的反应先结束,从另一方面看,消耗等量的金属,Fe产生的氢气比Zn产生的氢气多,因此正确的图形应该是 D、氢氧化钠先和溶液中的盐酸反应,一开始无沉淀产生,把盐酸消耗掉后,氢氧化钠和氯化铜反应生成沉淀,故D正确. 故选C. |
| 点评: | 本题通过坐标的形式考查了常见物质的性质,正确辨别坐标所表示的意义及坐标所表示的量的关系是解决问题的关键. |

 名校课堂系列答案
名校课堂系列答案已知:“”、“”和“”表示不同元素的原子.某反应的微观示意图如图,关于乙的构成说法合理的是( )
|
| A. | 只含和 | B. | 含有和 | C. | 只含 | D. | 只含 |
用CO还原铁的氧化物1.00g,得到铁粉0.75g,则下列说法中正确的是( )
|
| A. | 该氧化物是Fe2O3 |
|
| B. | 该氧化物可能是由FeO、Fe2O3、Fe3O4组成的混合物 |
|
| C. | 该氧化物是FeO |
|
| D. | 该氧化物中不含FeO |
 ,故C错误;
,故C错误; 个变化可以表示为:酒精 + 氧气
个变化可以表示为:酒精 + 氧气  二氧化碳 + 水 ,下列说法中正确的是 ( )
二氧化碳 + 水 ,下列说法中正确的是 ( ) 

 。
。