题目内容
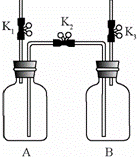
利用下图装置进行实验.实验前K1、K2、K3均已关闭.
| 内容 装置 | 实验1制备气体 | 实验2测定气体含量 |
|
| Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在K1上方导管口收集气体 | Ⅰ.A(容积350mL)中为用排空气法收集的CO2,B中装满水.用注射器向A中注入15mL NaOH溶液(足量),充分反应 Ⅱ.打开K2和K3 |
(1)检查装置气密性:保持K1关闭,打开K2、K3,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置在左侧气密性良好的现象是 ;用同样原理可以检查装置另一侧的气密性.
(2)实验1中,锌与稀硫酸反应的化学方程式为 ;气体收集完毕后,在不拆卸装置的情况下,使A中未反应的稀硫酸大部分转移到B中的操作是 .
(3)实验2中,当B中液面不再变化时,测得B中减少了160mL水,则A中CO2的体积分数约为 %.
考点:
氢气的制取和检验;检查装置的气密性;碱的化学性质;书写化学方程式、文字表达式、电离方程式.
专题:
常见的碱 碱的通性;常见气体的实验室制法、检验、干燥与净化.
分析:
(1)根据检查装置气密性的原理和方法来分析;
(2)锌与稀硫酸反应生成硫酸锌和氢气,通过改变装置内的压强的方法来分析;
(3)根据液体减少的体积即为被吸收的二氧化碳来分析.
解答:
解:(1)检查装置气密性:保持K1关闭,打开K2、K3,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,A中气体体积膨胀,看到B装置左侧导管口有气泡冒出;用同样原理可以检查装置另一侧的气密性.故填:B装置左侧导管口有气泡冒出;
(2)锌与稀硫酸反应生成硫酸锌和氢气,打开k2,k3,关闭k1,导致装置A中气体压强增大,稀硫酸被气体压入装置B中,
故填:Zn+H2SO4═ZnSO4+H2↑.打开k2,k3,关闭k1
(4)二氧化碳被氢氧化钠溶液完全吸收,气体减少的气体为:350mL﹣160mL﹣15mL=175mL.则A中CO2的体积分数约为: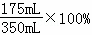 =50%;故填:50.
=50%;故填:50.
点评:
本题考查了装置气密性的检验、化学方程式的书写以及气体体积分数的计算,掌握化学基本知识是解题的关键.

一定温度下,一定质量的氢氧化钠固体溶于水制成溶液.下列有关的量不随水的质量改变而改变的是( )
|
| A. | 溶液质量分数 | B. | 溶液的pH |
|
| C. | 氢氧化钠的溶解度 | D. | 最多能吸收二氧化碳的质量 |
溶解度是解决溶液相关问题的重要依据.
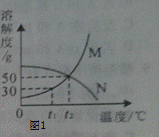
Ⅰ.根据图1解决下列问题:(M,N均不含结晶水)
(1)温度为 ℃时,M,N两种物质的溶解度相等;
(2)t1℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为 g.保持温度不变,向该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将 (填“变大”、“变小”或“不变”);
(3)t2℃时,将25gN加入50g水中,完全溶解后要提高该溶液的溶解质量分数,其操作方法是 .
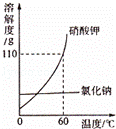
Ⅱ.根据表格解决实际问题:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 |
|
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 100 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 |
某KNO3样品中含有少量K2CO3,其提纯过程如图2: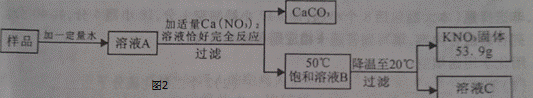
(1)图2中溶液C是 (填“饱和”或“不饱和”)溶液;
(2)样品中钾元素的质量为 g(结果保留整数).
下列关于物质用途的叙述,错误的是( )
|
| A. | 碳酸钙用作补钙剂 |
|
| B. | 二氧化碳用于制碳酸型饮料 |
|
| C. | 碳酸氢钠用于焙制糕点 |
|
| D. | 氢氧化钠用于干燥二氧化碳气体 |
下表各选项中,实验操作一定能够达到相对应的实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证氧气能支持燃烧 | 把带火星的木条伸到盛有氧气的集气瓶中 |
| B | 验证二氧化碳与水反应生成碳酸 | 向收集满二氧化碳的集气瓶中加入约 |
| C | 探究稀硫酸与氢氧化钠溶液恰好完全反应 | 向稀硫酸与氢氧化钠溶液反应后所得的溶液中滴加硝酸钡溶液 |
| D | 探究人体吸入的空气与呼出的气体中二氧化碳含量的不同 | 常温下,同时分别向同体积的盛有空气样品和呼出气体样品的集气瓶中滴加相同滴数的饱和澄清石灰水,振荡 |
|
| A. | A | B. | B | C. | C | D. | D |
 子的原子结构示意图。
子的原子结构示意图。 B.
B. 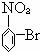 C.
C. 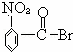 D.
D. 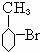
 体积的滴有酚酞的水,振荡
体积的滴有酚酞的水,振荡