题目内容
15.将15g镁、铁、锌混合物放入200g稀硫酸中恰好完全反应,然后对所得混合溶液在无氧条件下进行蒸发,得到63g不含结晶水的固体.则所用稀硫酸的溶质质量分数为( )| A. | 4.9% | B. | 9.8% | C. | 19.6% | D. | 24.5% |
分析 镁、锌、铁的混合物15g与足量的稀硫酸完全反应后,生成硫酸镁、硫酸锌、硫酸亚铁的混合物63g,根据反应前后元素质量不变,则硫酸镁、硫酸锌、硫酸亚铁三种物质的混合物中含硫酸根的质量为63g-15g=48g;根据硫酸根的质量计算硫酸的质量,进而求质量分数.
解答 解:镁、锌、铁的混合物15g与足量的稀硫酸完全反应后,生成硫酸镁、硫酸锌、硫酸亚铁的混合物63g,根据反应前后元素质量不变,则硫酸镁、硫酸锌、硫酸亚铁三种物质的混合物中含硫酸根的质量为63g-15g=48g,硫酸的化学式为H2SO4,则硫酸的质量为:$\frac{48g}{\frac{96}{98}×100%}$=49g,则所用稀硫酸的溶质质量分数为:
$\frac{49g}{200g}×100%$=24.5%
故选D.
点评 本题难度不是很大,顺利解题技巧在于:由金属元素和硫酸根组成的硫酸盐中,减去金属的质量即为硫酸根的质量.

练习册系列答案
相关题目
3.小明在实验操作技能考试中抽中的题目是:用固体氯化钠配制50g溶质质量分数为4%的氯化钠溶液.他的有关做法不正确的是( )
| A. | 计算得出需氯化钠2.0g,水48mL | |
| B. | 用托盘天平称量氯化钠2.0g,并将氯化钠倒入烧杯中溶解 | |
| C. | 配制好溶液后装瓶时发现有液体溅出,用水补充添加并贴上标签 | |
| D. | 实验完毕整理仪器、擦净桌 |
10.推理是化学学习中常见的思维方法.下列推理正确的是( )
| A. | 物质和氧气发生的反应属于氧化反应,所以发生氧化反应一定有氧气参加 | |
| B. | 某物质在氧气中燃烧后生成二氧化碳和水,则该物质中一定含有碳、氢、氧元素 | |
| C. | 向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,则该溶液中不一定存在SO42- | |
| D. | 不饱和溶液转化为饱和溶液后溶质质量分数一定增大 |
7.下列属于化学变化的是( )
| A. | 花瓶破碎 | B. | 水果榨汁 | C. | 铁锅生锈 | D. | 蜡烛熔化 |
4. 氢气、氦气均可用作飞艇的填充气.结合信息,回答下列问题.
氢气、氦气均可用作飞艇的填充气.结合信息,回答下列问题.
在0℃,1.01×105Pa时
(1)氢气曾用于飞艇的填充气,其原因是氢气的密度比空气小.
(2)目前使用氦气代替氢气,其理由是氦气的密度比空气小,化学性质稳定.
 氢气、氦气均可用作飞艇的填充气.结合信息,回答下列问题.
氢气、氦气均可用作飞艇的填充气.结合信息,回答下列问题.在0℃,1.01×105Pa时
| 空气 | 氢气 | 氦气 | |
| 密度/(g/L) | 1.293 | 0.0899 | 0.1786 |
(2)目前使用氦气代替氢气,其理由是氦气的密度比空气小,化学性质稳定.
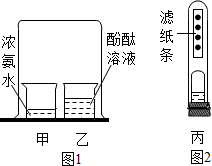 某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上. 关于图1、图2中的实验有以下说法,其中错误的是( )
某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上. 关于图1、图2中的实验有以下说法,其中错误的是( )