题目内容
8.请用化学方程式解释下列反应原理(1)用乙醇作燃料.
(2)水在直流电的作用下分解.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)乙醇燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(2)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故答案为:(1)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
18.下列四种金属中,其中一种与另外三种的颜色不同的是( )
| A. | 铁 | B. | 铝 | C. | 铜 | D. | 钛 |
19.碳元素与氧元素的本质区别是( )
| A. | 核外电子数不同 | B. | 核内质子数不同 | ||
| C. | 最外层电子数不同 | D. | 核内中子数不同 |
20.围绕“酸碱中和反应”,同学们分成若干小组,在老师引导下开展探究活动.
演示实验将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生疑问:反应后溶液中溶质是什么呢?
【假设猜想针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的,不合理的猜想是.
【实验探究】
(1)丙组同学取上述小烧杯中的溶液少量于试管中,滴加几滴Fe2(SO4)3溶液,无明显变化,溶液中一定没有.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.请填写实验现象:
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定,同时指出上述【实验探究
(2)中存在两处明显错误:
实验方案中的错误是BaC12与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4.
实验操作中的错误是pH试纸浸入溶液中.
演示实验将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生疑问:反应后溶液中溶质是什么呢?
【假设猜想针对疑问,大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的,不合理的猜想是.
【实验探究】
(1)丙组同学取上述小烧杯中的溶液少量于试管中,滴加几滴Fe2(SO4)3溶液,无明显变化,溶液中一定没有.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.请填写实验现象:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 | 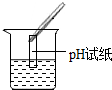 | 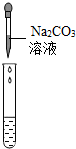 | 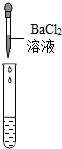 |
| 实验现象 | pH<7 | 有气泡 | 生成白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定,同时指出上述【实验探究
(2)中存在两处明显错误:
实验方案中的错误是BaC12与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4.
实验操作中的错误是pH试纸浸入溶液中.
18.下列成语蕴含的变化属于化学变化的是.( )
| A. | 刻舟求剑 | B. | 滴水成冰 | C. | 死灰复燃 | D. | 花香四溢 |
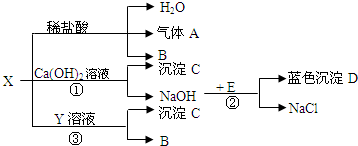
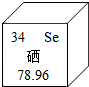 硒是人体必须的微量元素,如图是硒在元素周期表中的信息,由图可知硒的相对原子质量为78.96,硒原子的质子数为34.
硒是人体必须的微量元素,如图是硒在元素周期表中的信息,由图可知硒的相对原子质量为78.96,硒原子的质子数为34.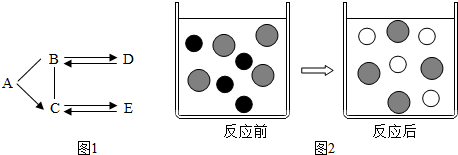
 Cu2+、
Cu2+、 SO42-、
SO42-、 Fe2+(填离子符号).
Fe2+(填离子符号).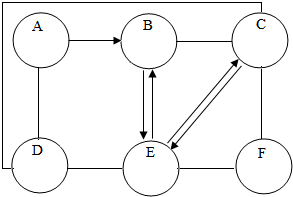 现有A、B、C、D、E、F六种初中化学常见的物质,分别是Fe2O3、盐酸、Na2CO3溶液、NaOH溶液、FeSO4溶液和CO2的一种物质,其中A是红棕色固体,D是胃酸的成分,E可以用于蒸馒头.用两圆间的短线“-”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:
现有A、B、C、D、E、F六种初中化学常见的物质,分别是Fe2O3、盐酸、Na2CO3溶液、NaOH溶液、FeSO4溶液和CO2的一种物质,其中A是红棕色固体,D是胃酸的成分,E可以用于蒸馒头.用两圆间的短线“-”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题: