题目内容
7.如图是实验室制取气体的常用装置.请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用的发生装置是A (填字母序号),该反应的符号表达式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)若用装置D收集氧气,验满方法是将带 火星的木条放于瓶口,若木条复燃则满.
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C装置作发生装置,请说明与B装置相比,C装置的优点是什么?可控制反应速率.在此反应中二氧化锰的作用是催化作用.
(4)若用装置E用排空气法收集氧气,则气体从a(填“a”或“b”)端通入;若用装置E用排水法收集氧气,先将瓶中装满水,正放桌面,再将气体从b(填“a”或“b”)端通入.
(5)高锰酸钾在医院常用作消毒剂.请计算(写出计算过程):
①高锰酸钾中钾、锰、氧元素的质量比;
②15.8g高锰酸钾所含氧元素的质量是多少?
分析 (1)加热高锰酸钾属于固体加热型,故选发生装置A,并据反应原理书写符号表达式;
(2)验满氧气的方法是:将带火星的木条放于瓶口,观察木条是否复燃进行判断;
(3)C装置中分液漏斗可控制液体的滴加速度,进而可控制反应速率,二氧化锰是反应的催化剂,起催化作用;
(4)氧气密度比空气大,故应从长管进气,其密度比水小,所以从短管进气,长管便于排水;
(5)①元素的质量比=相对原子质量与相应原子个数的乘积比;
②化合物中某元素的质量=该化合物的质量×该化合物中该元素的质量分数.
解答 解:(1)加热高锰酸钾属于固体加热型,故选发生装置A,反应的符号表达式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)验满氧气的方法是:将带火星的木条放于瓶口,观察木条是否复燃进行判断;
(3)C装置中分液漏斗可控制液体的滴加速度,进而可控制反应速率,二氧化锰是反应的催化剂,起催化作用;
(4)氧气密度比空气大,故应从长管进气,其密度比水小,所以从短管进气,长管便于排水;
(5)①高锰酸钾中钾、锰、氧元素的质量比是:39:55:(16×3)=39:55:48;
②15.8g高锰酸钾所含氧元素的质量是:15.8g×$\frac{16×3}{39+35.5+16×3}$×100%=4.8g;
故答案为:(1)A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)将带 火星的木条放于瓶口,若木条复燃则满;
(3)可控制反应速率;催化作用;
(4)a;b;
(5)①高锰酸钾中钾、锰、氧元素的质量比是:39:55:48;
②15.8g高锰酸钾所含氧元素的质量是4.8g.
点评 本题考查了实验室制取氧气的反应原理、验满方法、装置选取、据化学式的计算方法等知识,能较好考查学生分析、解决问题的能力.

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案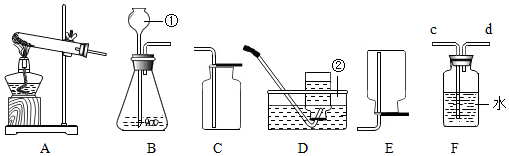
 回答有关用红磷测定空气中氧气含量的实验中的几个问题:
回答有关用红磷测定空气中氧气含量的实验中的几个问题: