题目内容
某环保小组为了测定某工厂废水中硫酸的含量,取196克废水,用20%的氢氧化钠溶液处理,当消耗40克氢氧化钠溶液时,溶液呈中性.求该工厂的废水中硫酸的质量分数是多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:稀硫酸和氢氧化钠反应生成硫酸钠和水,根据氢氧化钠溶液的质量、质量分数可以计算硫酸的质量,进一步可以计算该工厂的废水中硫酸的质量分数.
解答:解:设硫酸的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
40gx20% x
=
,
x=9.8g,
该工厂的废水中硫酸的质量分数为:
×100%=5%,
答:该工厂的废水中硫酸的质量分数为5%.
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
40gx20% x
| 80 |
| 98 |
| 40gx20% |
| x |
x=9.8g,
该工厂的废水中硫酸的质量分数为:
| 9.8g |
| 196g |
答:该工厂的废水中硫酸的质量分数为5%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
下列关于实验现象的描述,正确的是( )
| A、红磷在空气中燃烧产生白色的烟雾 |
| B、铁丝在氧气中燃烧生成黑色的四氧化三铁 |
| C、木炭在氧气中燃烧生成黑色固体 |
| D、硫在氧气中燃烧发出蓝紫色的火焰 |

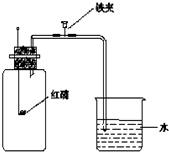 在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:
在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案: