题目内容
20.请帮助某同学完成知识卡片的内容专题:物质的类别性质和用途整理时间:2017年5月23日
| 化学式(物质名称) | 类别 | 性质 | 用途 |
| C(石墨) | ①单质 | 导电性 | 作电极 |
| ②NaHCO3 | 钠盐 | 能与酸反应 | 治疗胃酸过多 |
| H2SO4(浓硫酸) | 酸 | ③吸水性 | 干燥剂 |
| ④CO | 氧化物 | 还原性 | 冶炼金属 |
分析 物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可.
解答 解:石墨是由一种元素组成的纯净物,属于单质,能与酸反应且治疗胃酸过多的钠盐是碳酸氢钠,浓硫酸聚义吸水性,能用作干燥剂,能用于冶炼金属的具有还原性的氧化物是一氧化碳,故填:单质;NaHCO3;吸水性;CO;
点评 掌握物质的性质和用途的关系是正确解答本题的关键.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
1.中国是猕猴桃的原产地.猕猴桃是一种品质鲜嫩,营养丰富,风味鲜美的水果,有美容养颜、延迟皮肤衰老的效果.猕猴桃富含有的营养素是( )
| A. | 油脂 | B. | 维生素 | C. | 蛋白质 | D. | 无机盐 |
8.钠原子失去一个电子变为钠离子后,发生改变的是( )
| A. | 元素的种类 | B. | 钠的相对原子质量 | ||
| C. | 质子数 | D. | 微粒的电性 |
15.下列各组离子在水中一定能大量共存,并形成无色透明溶液的是( )
| A. | Cu2+、Fe2+、OH- | B. | H+、Cl-、CO32- | C. | K+、Ba2+、SO42- | D. | NH4+、Na+、NO3- |
5.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是( )
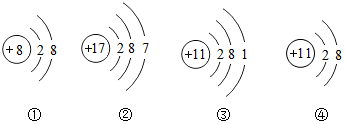

| A. | ④是一种阴离子 | B. | ③④属于同种元素 | ||
| C. | ①的化学性质比较稳定 | D. | ②容易得到电子 |
12.青蒿素(化学式C15H22O5)是抗疟药的有效成分.下列有关青蒿素说法正确的是( )
| A. | 青蒿素属于有机高分子化合物 | |
| B. | 青蒿素的相对分子质量为282 | |
| C. | 青蒿素中碳元素、氢元素、氧元素的个数比为15:22:5 | |
| D. | 青蒿素中氢元素的质量分数最大 |
9.某保健食品的外包装标签上的部分内容如下:
请回答下列问题
(1)该保健食品的主要功能是什么?.
(2)食用方法中嚼食的作用是什么?增大反应物的接触面积,促进钙的吸收.
(3)该保健品中的碳酸钙可以用石灰石来制备.第二小组同学设计了一种制备碳酸钙的实验方案,流程图为;

请写出上述方案有关反应的化学方程式:
①:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
②:CaO+H2O═Ca(OH)2.
③:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(4)怎样检验该保健食品是否含有碳酸盐?取保健食品加入试管中,然后滴加稀盐酸,观察到有气泡产生,将产生的气体通入澄清的石灰水中,石灰水变浑浊,说明有碳酸盐.
| 主要原料:碳酸钙 使用方法:每日1次,每次1片,嚼食. |
(1)该保健食品的主要功能是什么?.
(2)食用方法中嚼食的作用是什么?增大反应物的接触面积,促进钙的吸收.
(3)该保健品中的碳酸钙可以用石灰石来制备.第二小组同学设计了一种制备碳酸钙的实验方案,流程图为;

请写出上述方案有关反应的化学方程式:
①:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
②:CaO+H2O═Ca(OH)2.
③:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(4)怎样检验该保健食品是否含有碳酸盐?取保健食品加入试管中,然后滴加稀盐酸,观察到有气泡产生,将产生的气体通入澄清的石灰水中,石灰水变浑浊,说明有碳酸盐.
10.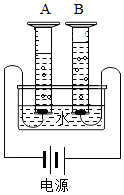 电解水时,加入少量氢氧化钠可以增强水的导电性(如图所示).现将一定质量0.1%的氢氧化钠溶液通电一段时间后,下列说法正确的是( )
电解水时,加入少量氢氧化钠可以增强水的导电性(如图所示).现将一定质量0.1%的氢氧化钠溶液通电一段时间后,下列说法正确的是( )
 电解水时,加入少量氢氧化钠可以增强水的导电性(如图所示).现将一定质量0.1%的氢氧化钠溶液通电一段时间后,下列说法正确的是( )
电解水时,加入少量氢氧化钠可以增强水的导电性(如图所示).现将一定质量0.1%的氢氧化钠溶液通电一段时间后,下列说法正确的是( )| A. | A中收集到的是氧气 | |
| B. | 溶液中氢氧化钠质量分数不变 | |
| C. | A中产生气泡速度比B中快 | |
| D. | 溶液减少的体积就是产生气体的体积 |
 太阳能路灯是利用太阳能进行照明的装置(如图),主要由太阳电池板、蓄电池、LED路灯灯头、灯珠和微电脑控制器这五大部分组成.
太阳能路灯是利用太阳能进行照明的装置(如图),主要由太阳电池板、蓄电池、LED路灯灯头、灯珠和微电脑控制器这五大部分组成.