题目内容
质量守恒定律是化学反应中的重要规律,我能运用此规律解答下列问题:
(1)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+3O2=2CO2+3H2O(反应条件已略去),则X的化学式为 C2H4 .
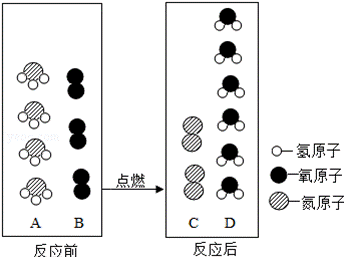
(2)在催化剂并加热的条件下,A与B反应生成C和D.反应前后分子变化的微观示意图所下所示:
①下列说法正确的是 (填序号).
a、该反应类型为置换反应
b、4种物质中只有D属于氧化物
c、反应前后,氮元素化合价升高
d、化学反应中分子可以再分,而原子不能
②该反应的化学方程式为 .
| 质量守恒定律及其应用;从组成上识别氧化物;微粒观点及模型图的应用;有关元素化合价的计算;化学反应的实质;反应类型的判定;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 化学反应模拟图型;化学用语和质量守恒定律. |
| 分析: | (1)根据反应前后原子的种类和数目都不变进行解答. (2)首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微粒数目关系,写出反应的方程式,然后再对题中各问加以分析解答. |
| 解答: | 解:(1)根据反应前后原子的种类和数目都不变:X+3O2═2CO2+2H2O,可以知道反应后有2个C,4个H,6个O,而反应前只出现了6个O,故X中含有2个C,4个H,化学式为C2H4. (2)解:将图对应成微粒相等如图:
化学方程式为:4NH3+3O2 a、根据置换反应是指一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应,故a正确; b、根据氧化物是指由两种元素组成,其中一种为氧元素的化合物,可知b正确; c、反应前,氮元素显﹣3价,反应后,氮元素显0价,故c正确; d、化学反应中分子可以再分,而原子不能再分正确; 故选abcd 故答案为:(1)C2H4 (2)①abcd ②4NH3+3O2 |
| 点评: | 本题综合性较强,但由于问题较多,容易被弄糊涂了,因此要从概念的科学定义出发,逐一解答.对于方程式书写的解答要注意配平,不能光看图示,否则容易出错. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案除去溶液中的少量杂质,试剂选择正确的是
| 选项 | 溶液 | 杂质 | 试剂 |
| A | NaNO3 | Na2CO3 | 适量BaCl2溶液 |
| B | CaCl2 | 稀盐酸 | 足量CaCO3固体 |
| C | ZnSO4 | CuSO4 | 足量铜粉 |
| D | Fe2(SO4)3 | Na2SO4 | 足量NaOH溶液 |
比较推理是化学学习中常用的思维方法,下列推理正确的是( )
|
| A. | 生铁比纯铁硬,故黄铜比纯铜硬 |
|
| B. | 烧碱属于碱,故纯碱也属于碱 |
|
| C. | 金刚石很硬,故石墨也很硬 |
|
| D. | 氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多 |
除去下列各物质中混有的少量杂质(括号内为杂质),所用除杂试剂及操作方法均正确的是( )
| 选项 | 物质 | 试剂 | 操作方法 |
| A | CO2(CO) | O2 | 点燃 |
| B | NaCl溶液(Na2SO4) | Ba(NO2)2溶液 | 先加入适量Ba(NO2)2,溶液后过滤 |
| C | CaO(CaCO3) | 稀盐酸 | 滴加适量稀盐酸 |
| D | Cu(Fe) | 稀硫酸 | 先加入适量稀硫酸,再过滤、洗涤、干燥 |
|
| A. | A | B. | B | C. | C | D. | D |
如图为某反应的微观示意图,不同的球代表不同的元素的原子,下列说法错误的是( )

|
| A. | 该反应属于分解反应 |
|
| B. | 该反应生成物全部为化合物 |
|
| C. | 该反应前后原子的种类、数目都未改变 |
|
| D. | 该图示能表示双氧水制取氧气的反应 |
 2N2+6H2O
2N2+6H2O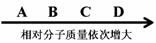 A、B、C、D是初中化学涉及到的不同物质,它们的相对分子质量依次增大(
A、B、C、D是初中化学涉及到的不同物质,它们的相对分子质量依次增大( 如下图所示)。请根据以下每个问题的具体情况分别进行回答。
如下图所示)。请根据以下每个问题的具体情况分别进行回答。 ,A可能的化学式为 (写出2个即可)。
,A可能的化学式为 (写出2个即可)。