题目内容
19.我国药学家屠呦呦因研究青蒿素获得2015年诺贝尔医学奖.青嵩素的化学式为Cl5H22O5,下列说法正确的是( )| A. | 青蒿素分子由三种元素组成 | B. | 青蒿素是一种有机物 | ||
| C. | 青蒿素含有42个原子 | D. | 青蒿素中氢元素的质量分数最大 |
分析 A.根据物质的组成和结构来分析;
B.根据有机物的概念来分析;
C.根据青蒿素的结构来分析;
D.根据化合物中元素的质量比来分析.
解答 解:A.青蒿素分子是由碳、氢、氧三种原子构成的,青蒿素是由碳、氢、氧三种元素组成的,故错误;
B.青蒿素是含碳元素的化合物,属于有机化合物,故正确;
C.青蒿素是由分子构成的,而不是由原子直接构成的,故错误;
D.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,由此可见其中碳元素的质量分数最大,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义、有机物的特征等进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.化学与人类息息相关,人类越来越离不开化学.
(1)生活离不开化学.表中列举了生活中两种常见的清洁剂,且NaClO+2HCl═NaCl+Cl2↑(黄绿色、有毒)+H2O,下列说法错误的是c(填序号)
a.“洁厕灵”可用于金属表面除锈
b.二者不能混合使用
c.NaClO中Cl元素的化合价是-1价.
(2)农作物增产依赖化学,NH4Cl、KCl、KNO3、Ca(H2PO4)2都是常用的化肥,其中KNO3属于复合肥.
(3)新药合成和发现依靠化学.我国女科学家屠呦呦因发现青蒿素荣获2015年诺贝尔科学或生理学奖.青蒿素(C15H22O5)是一种用于治疗疟疾的药物.
①一个青蒿素分子共有42个原子;
②青蒿素中C、H、O三种元素的质量比为90:11:40(最简整数比)
(1)生活离不开化学.表中列举了生活中两种常见的清洁剂,且NaClO+2HCl═NaCl+Cl2↑(黄绿色、有毒)+H2O,下列说法错误的是c(填序号)
| 清洁剂名称 | 洁厕灵 | 84消毒液 |
| 有效成分 | HCl | NaClO |
b.二者不能混合使用
c.NaClO中Cl元素的化合价是-1价.
(2)农作物增产依赖化学,NH4Cl、KCl、KNO3、Ca(H2PO4)2都是常用的化肥,其中KNO3属于复合肥.
(3)新药合成和发现依靠化学.我国女科学家屠呦呦因发现青蒿素荣获2015年诺贝尔科学或生理学奖.青蒿素(C15H22O5)是一种用于治疗疟疾的药物.
①一个青蒿素分子共有42个原子;
②青蒿素中C、H、O三种元素的质量比为90:11:40(最简整数比)
10.下列物质的用途中,利用其化学性质的是( )
| A. | 铜用于制作电线 | B. | 金刚石用来切割大理石 | ||
| C. | 干冰用于人工降雨 | D. | 熟石灰用来改良酸性土壤 |
7.空气中氮气的体积分数约为( )
| A. | 21% | B. | 0.03% | C. | 78% | D. | 0.94% |
14.下列关于金刚石的认识,错误的是( )
| A. | 质地较软 | B. | 由碳原子构成 | ||
| C. | 可做装饰品 | D. | 一定条件下能燃烧 |
11.图1是某兴趣小组在学习碱的性质时进行的探究活动,请要求回答问题.
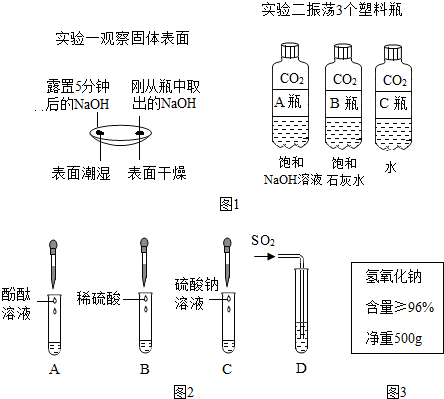
(1)通过分析实验一可知,氢氧化钠会吸收空气中的水蒸气.
(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起对比作用.
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入下列图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀.
①写出D试管中反应的化学方程式Ba(OH)2+SO2═BaSO3↓+H2O.
②不同的碱溶液中都含有OH-,所以,碱有一些相似的化学性质.上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是C(填字母序号)
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究.
【提出问题】氢氧化钠含有什么杂质
【提出猜想】
猜想I:查阅资料可知,工业用氢氧化钠可能含有NaCl.
猜想Ⅱ:工业用氢氧化钠可能含有Na2CO3,原因是氢氧化钠与空气中的二氧化碳反应生成碳酸钠(用简洁的文字表述).
【进行实验】

(1)通过分析实验一可知,氢氧化钠会吸收空气中的水蒸气.
(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起对比作用.
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入下列图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀.
①写出D试管中反应的化学方程式Ba(OH)2+SO2═BaSO3↓+H2O.
②不同的碱溶液中都含有OH-,所以,碱有一些相似的化学性质.上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是C(填字母序号)
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究.
【提出问题】氢氧化钠含有什么杂质
【提出猜想】
猜想I:查阅资料可知,工业用氢氧化钠可能含有NaCl.
猜想Ⅱ:工业用氢氧化钠可能含有Na2CO3,原因是氢氧化钠与空气中的二氧化碳反应生成碳酸钠(用简洁的文字表述).
【进行实验】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量固体样品于试管中,加水溶解 | 固体全部溶解 | / |
| ②向①所得溶液中滴加过量的硝酸 | 一开始无明显变化,一会儿后产生能使澄清石灰水变浑浊的气体 | 样品中含有Na2C03 |
| ③向②所得溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有NaCl.反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3 |
16.10.6克不纯碳酸钠样品与足量盐酸反应后,共得到4.4g二氧化碳,则不纯碳酸钠中所含杂质可能是下列选项中的( )
| A. | CaCO3和K2CO3 | B. | MgCO3和CaCO3 | C. | K2CO3和ZnCO3 | D. | ZnCO3和Ag2CO3 |
 已知A、B、C、D、E为初中化学中常见的五种不同类型的物质,其中A为年产量最高的金属单质,各种物质间的反应和转化关系如图所示 (“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质:反应条件、部分反应物和生成物已略去).请回答:
已知A、B、C、D、E为初中化学中常见的五种不同类型的物质,其中A为年产量最高的金属单质,各种物质间的反应和转化关系如图所示 (“一”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质:反应条件、部分反应物和生成物已略去).请回答: