题目内容
2.如图所示实验室中常见的气体制备、干燥、收集和性质实验的部分装置(组装实验装置时,可重复选择).试根据题目要求.回答下列问题: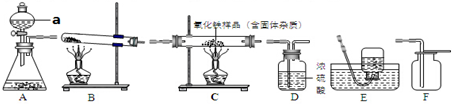
Ⅰ.氯酸钾(KClO3)固体在二氧化锰做催化剂并加热的条件下,能较快的分解为氯化钾和氧气.小刚同学欲在实验室中以此方法制备并收集干燥的氧气.
(1)所选仪器的连接顺序为B→D→F(填写仪器序号字母).
(2)用氯酸钾制备氧气所发生的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
Ⅱ.小强同学欲用锌和稀硫酸反应制取氢气,然后利用氢气测定某氧化铁样品中含Fe2O3的质量分数(假设杂质不发生反应).选择氢气的发生装置是A,接下来连接装置
的连接顺序为:D1→C→D2→D3.(已知:Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O;其中D1、D2、D3为三个浓硫酸洗气瓶)
(1)写出仪器a的名称分液漏斗,在装药品之前,检查仪器A气密性的具体操作步骤是关闭分液漏斗的开关,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,如果导管口有气泡冒出,证明气密性良好.
(2)小强欲通过测量反应前后D2浓硫酸洗气瓶的质量变化,测算氧化铁样品中含有Fe2O3的质量分数.实验中,在其他操作正常的条件下,若装置中不连接D1,则测算结果将偏大.(填写“偏小”“偏大”“不受影响”).
分析 Ⅰ.
(1)收集干燥的氧气,所以要先制取,再干燥,再收集;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气,据此书写方程式;
Ⅱ.
(1)据常用仪器和检查气密性的方法分析解答;
(2)制取的氢气中含有水蒸气,如果不除去水蒸气,会导致计算出的氧化铁样品的纯度偏大.
解答 解:Ⅰ.(1)如果用氯酸钾制氧气就需要加热,氧气可以用浓硫酸干燥,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用向上排空气法收集的氧气比较纯净;
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
Ⅱ.(1)标号仪器是分液漏斗,可以控制反应的发生和停止;检查仪器A气密性的具体操作步骤是:关闭分液漏斗的开关,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,如果导管口有气泡冒出,证明装置气密性良好;
(2)实验中,在其他操作正常的条件下,若装置中不连接D1,则测算结果将偏大,因为没有D1时,氢气中混有的水蒸气被D2吸收,结果偏大;
故答案为:
(1)B→D→F.(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
Ⅱ. (1)分液漏斗;关闭分液漏斗的开关,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,如果导管口有气泡冒出,证明气密性良好;
(2)偏大.
点评 本考点主要考查了仪器的连接和气体的除杂和干燥,同时也考查了化学方程式的书写,混合物中物质质量分数的测定等知识,综合性比较强,要结合所学知识细心分析解答.

练习册系列答案
相关题目
12.夏时制又称“日光节约时制”和“夏令时间”,在天亮早的夏季人为将时间提前一小时,可以充分利用光照资源,从而节约照明时间,减少资源消耗,下列做法不符合这一主题的是( )
| A. | 防铁生锈 | B. | 回收塑料 | C. | 随手关灯 | D. | 以车代步 |
13.下列关于CO和CO2说法正确的是( )
| A. | CO和CO2均可由含碳物质燃烧生成 | |
| B. | CO2在任何情况下都不能支持燃烧 | |
| C. | CO只有氧化性 | |
| D. | CO和CO2组成元素相同,化学性质相同 |
17.汶川震后防疫使用的一种高效消毒剂的主要成分为三氯异氰尿酸(C3O3N3Cl3),又称高氯精.下列有关高氯精的说法不正确的是( )
| A. | 高氯精由4种元素组成 | |
| B. | 高氯精分子中C、O、N、Cl的原子个数比为1:1:1:1 | |
| C. | 高氯精中C、N两种元素的质量比为6:7 | |
| D. | 高氯精是由C、O、N、Cl四种原子构成 |
7.缉毒犬能根据气味发现毒品,这说明( )
| A. | 分子很小 | B. | 分子是可分的 | C. | 分子之间有间隔 | D. | 分子在不断运动 |
11.在一个密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如表:
且X的相对分子质量为n,Q的相对分子质量为2n,则下列推理不正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 12 | 15 | 待测 |
| A. | 该反应不可能是分解反应 | |
| B. | 反应后生成14gZ | |
| C. | 参加反应的X与Q的质量比是1:3 | |
| D. | 该反应方程式中X与Q的化学计量数比为3:2 |
12.向盛有碳酸钠溶液(滴有少量无色酚酞溶液)的烧杯中逐滴加入稀盐酸,在不同阶段测定所得溶液的pH和蒸干所得白色固体成分进行分析,下列说法不正确的是( )
| A. | 若反应后的溶液的 pH≤7,蒸干后得到的白色固体只有氯化钠 | |
| B. | 向白色固体中滴入稀盐酸,有气泡说明原反应后的溶液 pH>7 | |
| C. | 若反应后的溶液显无色,说明稀盐酸和碳酸钠恰好完全反应 | |
| D. | 当没有气泡产生时,说明稀盐酸和碳酸钠恰好完全反应 |
 我国著名化学家侯德邦先生发明的“侯氏制碱法”,不仅使我国制碱工业得到极大进步,而且促进了世界制碱技术.
我国著名化学家侯德邦先生发明的“侯氏制碱法”,不仅使我国制碱工业得到极大进步,而且促进了世界制碱技术.