��Ŀ����
9��������ͼ1����Ϣ�ش����⣮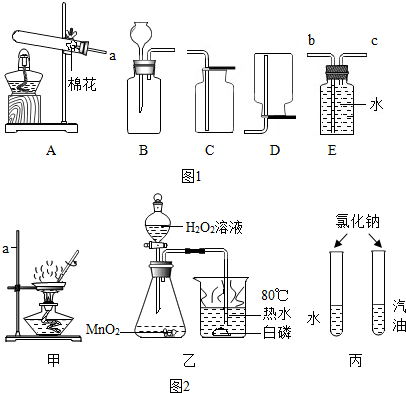
װ�ü�ҩƷ����ʯ��ʯ ��ϡ���� �۶������� �ܸ������ ��ϡ���� ����������Һ
��1��СӢͬѧѡ��Aװ����ȡ��������Ӧ�Ļ�ѧ����ʽΪ2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2������ѡ��Eװ���ռ���������a��Ӧ��c��������
��2��С��ͬѧ����ʵ������ȡ������̼������ѡ���ҩƷ�Ǣ٢ݣ�����ţ�����Cװ���ռ�������̼��֤��������̼���ռ����ķ����ǽ�ȼ�ŵ�ľ����������ƿ�ڣ���ľ��Ϩ����˵��������̼���ռ�����
��3������������Һ��ʵ�飬����a������������̨���ò��������Ͻ����Ŀ����ʹ���Ⱦ��ȣ���ֹ�ֲ����ȣ�Һ�ηɽ���
��4������̽��ȼ��������ʵ�飬��Һ©���Ļ���ǰ�����ײ�ȼ�գ�������ȼ�գ��Ƚϴ�ǰ�������֤������ȼ����Ҫ�������ձ���ˮ���������ṩ������ʹ�¶ȴﵽ�����Ż�㣻����������
��5������һ��Ա�ʵ�飬ʵ��Ŀ���ǶԱ��Ȼ�����ˮ�������е��ܽ�Ȳ�ͬ��
���� ��1�������������ʱ�ܹ��ֽ���������ء��������̺�������
Ϊ�˷�ֹ������ؽ��뵼�ܣ�ͨ�����Թܿ���һ������
��2��ʵ����ͨ���ô���ʯ��ʯ��ʯ��ϡ���ᷴӦ��ȡ������̼����Ӧ����Ҫ���ȣ�����ʯ��ʯ��ʯ����Ҫ�ɷ���̼��ƣ��ܺ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��
������̼�ܹ�����ˮ���ܶȱȿ�������ȼ�գ���֧��ȼ�գ�
��3������������;�н��衢������ת�����ʵȣ�
��4����ȼ��ȼ�յ������ǣ��������Ӵ����¶ȴﵽ��ȼ����Ż�㣬���߱���ͬʱ�߱���ȱһ���ɣ�
��5��ͬ�������ڲ�ͬ���ܼ����ܽ�������ͬ��
��� �⣺��1��ѡ��Aװ����ȡ����ʱ�������Թܿ���һ������Ӧ�������ø��������ȡ��������Ӧ�Ļ�ѧ����ʽΪ��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2����
ѡ��Eװ���ռ���������a��Ӧ��c��������
���2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2����c��
��2����ʵ������ȡ������̼ʱ��ѡ���ҩƷ��ʯ��ʯ��ϡ���
������̼�ܹ�����ˮ����������ˮ���ռ����ܶȱȿ��������������ſ������ռ�������Cװ���ռ���
֤��������̼���ռ����ķ����ǣ���ȼ�ŵ�ľ����������ƿ�ڣ���ľ��Ϩ����˵��������̼���ռ�����
����٢ݣ�C����ȼ�ŵ�ľ����������ƿ�ڣ���ľ��Ϩ����˵��������̼���ռ�����
��3������������Һ��ʵ�飬����a������������̨���ò��������Ͻ����Ŀ���ǣ�ʹ���Ⱦ��ȣ���ֹ�ֲ����ȣ�Һ�ηɽ���
�������̨��ʹ���Ⱦ��ȣ���ֹ�ֲ����ȣ�Һ�ηɽ���
��4���Ƚϴ�ǰ�������֤������ȼ����Ҫ�������ձ���ˮ�������ǣ��ṩ������ʹ�¶ȴﵽ�����Ż�㣻����������
����������ṩ������ʹ�¶ȴﵽ�����Ż�㣻����������
��5������һ��Ա�ʵ�飬ʵ��Ŀ���ǶԱ��Ȼ�����ˮ�������е��ܽ�Ȳ�ͬ��
����Ա��Ȼ�����ˮ�������е��ܽ�Ȳ�ͬ��
���� �������ʵ�飬��ѧ�ؽ���ʵ�顢����ʵ�飬�ǵó���ȷʵ����۵�ǰ�ᣬ���Ҫѧ�����ʵ�顢����ʵ�顢����ʵ�飬Ϊѧ�û�ѧ֪ʶ�춨������

���Ķ����ϡ�
��1��25��ʱ���������������pH��Χ�����
| Zn��OH��2 | Fe��OH��2 | Mg��OH��2 | |
| ��ʼ������pH | 5.7 | 7.6 | 10.4 |
| ������ȫ��pH | 8.0 | 9.6 | 12.4 |
��3���Ʊ�Fe3O4��ʵ��������ͼ��
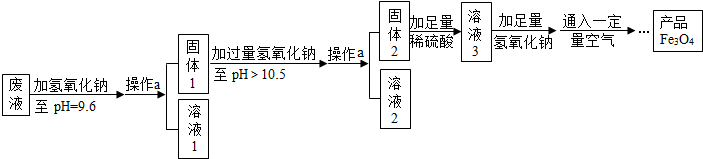
���ش����⡿
��1������Һ�м�������������Һ���ɳ����Ļ�ѧ����ʽΪ��дһ�����ɣ�2NaOH+ZnSO4�TZn��OH��2��+Na2SO4����2NaOH+FeSO4�TFe��OH��2��+Na2SO4����
��2����Һ1���������У�����д���֣�����þ�������ƣ���Һ3�������ʵ���Ҫ�ɷ�Ϊ����������
��3����ʵ��ȡ��Һ100g�����յõ���Ʒ��������������Ϊ2.32g����ԭ��Һ�������������ʵ���������������4.56%����ȷ��0.01%����
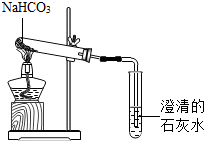 ����ͼ��ʾװ�ü���NaHCO3���Թ������µİ�ɫ����ֻ��Na2CO3�����۲쵽�Թ��ڱ���ˮ�����ɣ�����ʯ��ˮ����ǣ�����ʵ��ش����⣮
����ͼ��ʾװ�ü���NaHCO3���Թ������µİ�ɫ����ֻ��Na2CO3�����۲쵽�Թ��ڱ���ˮ�����ɣ�����ʯ��ˮ����ǣ�����ʵ��ش����⣮