题目内容
17.怎样检验暴露于空气中的氢氧化钠是否变质?取少量样品,向其中滴加稀盐酸,有气泡产生,将收集到的气体通入澄清的石灰水中,如果有白色沉淀生成,则证明氢氧化钠固体已变质
(1)氢氧化钠溶液长期放置在空气中(不考虑溶剂的蒸发),溶液的质量会增加,是因为:氢氧化钠溶液吸收了空气中的二氧化碳
(2)氢氧化钠固体放置在空气中,固体质量会增加,是因为:吸收空气中的水分发生潮解,还能吸收空气中的二氧化碳生成碳酸钠和水
(3)氢氧化钠吸收空气中的水分而潮解,易与二氧化碳反应而变质,所以应密封保存,并且要用橡胶塞.
分析 根据氢氧化钠的物理性质与化学性质进行分析必须密封保存的原因;氢氧化钠变质后生成的杂质是碳酸钠,因此检验是否变质即检验是否存在碳酸根离子;据此结合碳酸盐的检验方法(滴加盐酸,若产生气体,再检验气体能否使澄清石灰水变浑浊)进行分析解答.
解答 解:氢氧化钠能与空气中的二氧化碳反应生成碳酸钠和水,变质后生成的杂质是碳酸钠,因此检验是否变质即检验是否存在碳酸根离子;取少量样品,向其中滴加稀盐酸,有气泡产生,将收集到的气体通入澄清的石灰水中,如果有白色沉淀生成,则证明氢氧化钠固体已变质.
(1)氢氧化钠溶液长期放置在空气中(不考虑溶剂的蒸发),溶液的质量会增加,是因为吸收了空气中的二氧化碳,生成了碳酸钠和水.
(2)氢氧化钠固体放置在空气中,固体质量会增加,是因为能吸收空气中的水分发生潮解;还能与空气中的二氧化碳反应生成碳酸钠和水.
(3)氢氧化钠吸收空气中的水分而潮解,易与二氧化碳反应而变质,所以应密封保存,并且要用橡胶塞.
故答案为:稀盐酸;气泡;澄清的石灰水;白色沉淀生成;
(1)氢氧化钠溶液吸收了空气中的二氧化碳;(2)吸收空气中的水分发生潮解,还能吸收空气中的二氧化碳生成碳酸钠和水;(3)密封.
点评 本题难度不大,考查氢氧化钠的性质和碳酸盐的检验方法,掌握氢氧化钠的性质、碳酸盐的检验方法是正确解答本题的关键.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
8.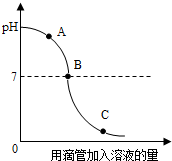 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线,下列有关该实验事实的说法正确的是( )| A. | 该实验是将氢氧化钠滴入盐酸溶液中 | |
| B. | A点时的溶液能使石蕊试液变红 | |
| C. | B点表示盐酸和氢氧化钠恰好完全反应 | |
| D. | C点时,溶液中的溶质只有氯化钠 |
12.下列物质的鉴别方法正确的是( )
| A. | 铁钉鉴别稀盐酸和稀硫酸 | |
| B. | 用硫酸铜溶液鉴别水和烧碱溶液 | |
| C. | 用酚酞溶液鉴别食盐水和稀盐酸 | |
| D. | 用烧碱溶液鉴别一氧化碳和二氧化碳 |
2.在硝酸银和硝酸铜的混合液中,加入一定量的铁粉后有少量金属析出,过滤后往滤渣中滴加盐酸,有气泡生成.则滤渣中的金属是( )
| A. | 铁 | B. | 银和铁 | C. | 铜和铁 | D. | 银、铜和铁 |
3.小明在实验室验证盐酸化学性质时,将碳酸钠溶液倒入装有稀盐酸的烧杯中看到有气泡产生.为了解两种物质间的反应情况,他决定从反应后溶液中溶质的组成入手进行探究.
(1)小明对反应后溶液溶质组成提出了三种猜想:
猜想1:溶质为NaCl和Na2CO3
猜想2:溶质为NaCl和HCl
补充猜想3:溶质为NaCl
(2)比较三种猜想,请你说出猜想3的理由:当碳酸钠与盐酸恰好完全反应时,生成氯化钠和水和二氧化碳,因此溶液中的溶质只有氯化钠
(3)小明设计两个不同的实验方案,用两种方法验证了猜想2成立.按要求填写下表.
(4)反思与评价:
你认为方法二是否正确不正确,说出理由:NaCl中也有氯离子,如果没有盐酸,也能产生白色沉淀.
(1)小明对反应后溶液溶质组成提出了三种猜想:
猜想1:溶质为NaCl和Na2CO3
猜想2:溶质为NaCl和HCl
补充猜想3:溶质为NaCl
(2)比较三种猜想,请你说出猜想3的理由:当碳酸钠与盐酸恰好完全反应时,生成氯化钠和水和二氧化碳,因此溶液中的溶质只有氯化钠
(3)小明设计两个不同的实验方案,用两种方法验证了猜想2成立.按要求填写下表.
| 实验操作 | 实验现象 | 实验结论 | |
| 方法一 | 取少量反应后溶液,加入锌粒 | 有气泡冒出 | 猜想2成立 |
| 方法二 | 取少量反应后溶液,加入硝酸银溶液 | 有白色沉淀生成 | 猜想2成立 |
你认为方法二是否正确不正确,说出理由:NaCl中也有氯离子,如果没有盐酸,也能产生白色沉淀.
20.某兴趣小组在学习碱的化学性质时,进行了如图所示的实验.
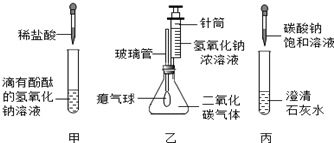
(1)乙中滴加氢氧化钠溶液后,可观察到现象是气球胀大,这是因为二氧化碳被氢氧化钠溶液吸收,瓶内压强减低,在外界大气压的作用下,气球膨胀起来.
(2)丙中观察到试管内有白色沉淀产生.
(3)结束后,同学们将甲、乙、丙三个废液倒入同一个干净废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【讨论交流】①一定含有物质:碳酸钙、指示剂、水和NaCl.
②还含有能使废液呈碱性物质.能使废液呈碱性物质是什么?同学们有如下猜想.
小兰认为:只有碳酸钠
小亮认为:是氢氧化钠和碳酸钠
你认为还可能是氢氧化钠.(写一种猜想)
【设计】小斌想用氯化钙溶液来验证以上猜想.查阅资料获悉氯化钙溶液呈中性,并设计如下.请你将小斌设计补充完整.
【反思拓展】分析化学反应后所得物质成分,除考虑生成物外还需考虑反应物是否有剩余.

(1)乙中滴加氢氧化钠溶液后,可观察到现象是气球胀大,这是因为二氧化碳被氢氧化钠溶液吸收,瓶内压强减低,在外界大气压的作用下,气球膨胀起来.
(2)丙中观察到试管内有白色沉淀产生.
(3)结束后,同学们将甲、乙、丙三个废液倒入同一个干净废液缸中,最终看到废液浑浊并呈红色,由此产生疑问.
【提出问题】废液中含有哪些物质?
【讨论交流】①一定含有物质:碳酸钙、指示剂、水和NaCl.
②还含有能使废液呈碱性物质.能使废液呈碱性物质是什么?同学们有如下猜想.
小兰认为:只有碳酸钠
小亮认为:是氢氧化钠和碳酸钠
你认为还可能是氢氧化钠.(写一种猜想)
【设计】小斌想用氯化钙溶液来验证以上猜想.查阅资料获悉氯化钙溶液呈中性,并设计如下.请你将小斌设计补充完整.
| 内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置 | 有白色沉淀,溶液由红色变为无色 | 小兰的猜想正确. |
| 有白色沉淀,溶液呈红色 | 小亮的猜想正确. |
1.下列说法不正确的是( )
| A. | 人类需要的大部分能量是由化学反应产生的 | |
| B. | 石油是由沸点不同的化合物组成的混合物 | |
| C. | 应不断加大化石燃料的开采力度以满足人类生产生活的需要 | |
| D. | 在化石燃料中,天然气是比较清洁的燃料 |