题目内容
19. 太阳能路灯系统是利用太阳能进行照明的装置,被越来越广泛地应用.它是由太阳能电池板、蓄电池、LED灯、灯柱、微电脑控制器这五大部分组成.
太阳能路灯系统是利用太阳能进行照明的装置,被越来越广泛地应用.它是由太阳能电池板、蓄电池、LED灯、灯柱、微电脑控制器这五大部分组成.(1)灯柱材料用铝合金而不用钢铁,原因之一是铝能跟空气中氧气反应,生成一层致密的氧化膜,具有很好的抗腐蚀性能,这一反应的化学方程式为:4Al+3O2=2Al2O3;铝合金属于混合物(选填“化合物”或“混合物”).
(2)蓄电池白天充电时发生的反应为:2PbSO4+2H2O=Pb+X+2H2SO4,则X的化学式为PbO2.
分析 (1)根据铝制品耐腐蚀主要是因为铝能与空气中的氧气反应生成一层致密氧化膜,写出反应的化学方程式即可以及根据铝合金的定义进行解答;
(2)根据质量守恒定律,化学反应前后元素的种类和原子的个数不变;
解答 解:(1)铝制品耐腐蚀主要是因为铝能与空气中的氧气反应生成一层致密氧化膜,反应的化学方程式为:4Al+3O2═2Al2O3.铝合金是铝和其他金属的混合物;“铝合金”是由铝与其它金属或非金属熔合而成的具有铝的性质的混合物.所以“铝合金”属于混合物;
(2)2PbSO4+2H2O═Pb+X+2H2SO4,反应前含有2个Pb原子,2个S原子,4个H原子,10个O原子,反应后含有1个Pb原子,4个H原子,2个S原子,8个O原子,故X中含有1个Pb原子,2个O原子,故其化学式为PbO2;
故答案为:(1)4Al+3O2=2Al2O3 混合物 (2)PbO2.
点评 本题难度不大,掌握金属铝耐腐蚀的原因、化学方程式的书写以及质量守恒定律是正确解答本题的关键

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列模型能表示氧气分子结构的是( )
| A. | 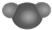 | B. |  | C. | 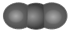 | D. | 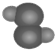 |
11.在下列生活和生产过程中,发生了化学变化的是( )
| A. | 矿石粉碎 | B. | 海水晒盐 | C. | 谷物酿酒 | D. | 石头雕像 |
14.现在有部分氧化的镁6.4克与100克14.6%稀盐酸恰好完全反应,产生的氢气质量为( )
| A. | 0.1g | B. | 0.2g | C. | 0.3g | D. | 0.4g |