题目内容
14.硝酸铵(NH4NO3)受撞击后受热后会发生爆炸性的分解,可用作炸药.又因其含氮量比较高,也用作化肥.试计算:(1)硝酸铵的相对分子质量80;
(2)硝酸铵中氮元素与氢元素的质量比为7:1;
(3)计算100克硝酸铵中氮元素的质量?(写出计算过程)
分析 (1)根据相对分子的质量(式量)为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据物质中某元素的质量=该物质×物质中某元素的质量分数,进行解答.
解答 解:(1)根据相对分子的质量(式量)为组成分子的各原子的相对原子质量之和,可得硝酸铵的相对分子质量为14×2+4+16×3=80.
故答案为:80;
(2)硝酸铵中氮、氢元素的质量之比是(14×2):(4×1)=7:1.
故答案为:7:1.
(3)根据物质中某元素的质量=该物质×物质中某元素的质量分数,可得100g硝酸铵中含氮元素的质量为:
100g×$\frac{14×2}{80}$×100%=35g.
答:100克硝酸铵中氮元素的质量是35g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
2.下列说法正确的是( )
| A. | 生活中常用蒸馏的方法将硬水软化 | |
| B. | 可用带火星的木条鉴别空气、氧气和二氧化碳 | |
| C. | 用冷碟子放在蜡烛火焰上方制炭黑 | |
| D. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 |
5.下列对分子、原子、离子的认识,不正确的是( )
| A. | 远处可以闻到花的香味是因为分子间有间隙 | |
| B. | 湿衣服晾干是因为水分子不断运动 | |
| C. | 分子、原子、离子都可以构成物质 | |
| D. | 由分子构成的物质,分子是保持物质化学性质的最小粒子 |
2.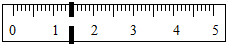 某同学用托盘天平称量物质的质量,左盘砝码的质量为5g,游码的读数如图所示,则下列结论正确的是( )
某同学用托盘天平称量物质的质量,左盘砝码的质量为5g,游码的读数如图所示,则下列结论正确的是( )
 某同学用托盘天平称量物质的质量,左盘砝码的质量为5g,游码的读数如图所示,则下列结论正确的是( )
某同学用托盘天平称量物质的质量,左盘砝码的质量为5g,游码的读数如图所示,则下列结论正确的是( )| A. | 操作错误,无法称量 | B. | 物质质量为5.4 g | ||
| C. | 物质质量为3.6 g | D. | 物质质量为6.4 g |
19.下列实验操作正确的是( )
| A. |  氧气的验满 | B. |  气密性的检查 | C. |  熄灭酒精灯 | D. |  闻气体的气味 |
4.下列化学用语书写正确的是( )
| A. | 1个氖原子 Na | B. | +2价的铁元素 Fe+2 | ||
| C. | 4个氢分子 4H | D. | 3个碳酸根离子 3CO32- |