题目内容
3.下列生产、生活中的变化,都属于化学变化的是( )| A. | 冰块融化、食物霉变 | B. | 海水晒盐、糯米酿酒 | ||
| C. | 铁锅生锈、光合作用 | D. | 电灯发光、酒精挥发 |
分析 化学变化是指有新物质生成的变化.物理变化是指没有新物质生成的变化.化学变化和物理变化的本质区别是否有新物质生成.
解答 解:A、冰块融化的过程中没有新物质生成,属于物理变化;
B、海水晒盐的过程中没有新物质生成,属于物理变化;
C、铁锅生锈过程中有新物质铁锈生成,属于化学变化;光合作用过程中有新物质氧气等生成,属于化学变化;
D、电灯发光的过程中没有新物质生成,属于物理变化;酒精挥发的过程中没有新物质生成,属于物理变化.
故选C.
点评 本题主要考查了物理变化和化学变化,可以依据化学变化的实质进行.

练习册系列答案
相关题目
13.果糖(化学式:C6H12O6)大量存在于水果中,下列有关果糖的说法不正确的是( )
| A. | 属于有机化合物 | |
| B. | 果糖中碳、氢、氧三种元素的质量比为1:2:1 | |
| C. | 一个果糖分子由24个原子构成 | |
| D. | 果糖由碳、氢、氧三种元素组成 |
11.下列除去杂质的试剂和方法可行的是( )
| 选项 | 物质(括号内为杂质) | 除杂试剂和方法 |
| A | CO2(CO) | 通过足量澄清石灰水 |
| B | N2(O2) | 通过灼热的氧化铜 |
| C | Mg(NO3)2溶液(AgNO3) | 加入过量铁粉,过滤 |
| D | NaCl溶液(Na2SO4) | 加入适量BaCl2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
18. 小明是位爱思考的同学.他想:二氧化碳与澄清石灰水反应可以有明显现象,如何使二氧化碳与氢氧化钠的反应也产生明显现象呢?
小明是位爱思考的同学.他想:二氧化碳与澄清石灰水反应可以有明显现象,如何使二氧化碳与氢氧化钠的反应也产生明显现象呢?
【查阅资料】
表一:NaOH、Na2CO3和NaCl在水的溶解度(用s表示)
表二:NaOH、Na2CO3和NaCl在乙醇的溶解度(用s表示)
【实验设计】
(1)实验装置:如图
(2)实验过程:(a)称取8g NaOH固体于烧杯中,加进50mL95%乙醇,不断搅拌,使其成饱和氢氧化钠的乙醇溶液,倒入试剂瓶中备用.(b)取20mL饱和氢氧化钠的乙醇溶液于具支试管中,通入CO2,直至产生粘稠的白色胶状沉淀物.
【实验交流】
(1)表一中“51”的意义是:“51”表示在10℃时,NaOH固体在100g水中最多能溶解51g.
(2)写出实验中“产生粘稠的白色胶状沉淀物”的反应方程式CO2+2NaOH═Na2CO3↓+H2O.
(3)装置图中的“稀盐酸”你认为它的作用是:检验白色胶状沉淀物是Na2CO3.为了证明你的结论你觉得该添加的装置为 (请画在上面装置图中,并请注明所需要的试剂).
(请画在上面装置图中,并请注明所需要的试剂).
(4)这个实验给你体会最深的一点:相同的溶质在不同的溶剂里溶解度不同;改变传统实验采用水作溶剂的思路,反应可选择其它的溶剂(答案合理即可).
 小明是位爱思考的同学.他想:二氧化碳与澄清石灰水反应可以有明显现象,如何使二氧化碳与氢氧化钠的反应也产生明显现象呢?
小明是位爱思考的同学.他想:二氧化碳与澄清石灰水反应可以有明显现象,如何使二氧化碳与氢氧化钠的反应也产生明显现象呢?【查阅资料】
表一:NaOH、Na2CO3和NaCl在水的溶解度(用s表示)
| T/℃ | s(NaOH) | s(Na2CO3) | s(NaCl) |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36 |
| 25 | 105.3 | 29.4 | 36.1 |
| 30 | 119 | 39.7 | 36.3 |
| T/℃ | s(NaOH) | s(Na2CO3) | s(NaCl) |
| 18.5-25.0 | 17.3 | -- | 0.1 |
(1)实验装置:如图
(2)实验过程:(a)称取8g NaOH固体于烧杯中,加进50mL95%乙醇,不断搅拌,使其成饱和氢氧化钠的乙醇溶液,倒入试剂瓶中备用.(b)取20mL饱和氢氧化钠的乙醇溶液于具支试管中,通入CO2,直至产生粘稠的白色胶状沉淀物.
【实验交流】
(1)表一中“51”的意义是:“51”表示在10℃时,NaOH固体在100g水中最多能溶解51g.
(2)写出实验中“产生粘稠的白色胶状沉淀物”的反应方程式CO2+2NaOH═Na2CO3↓+H2O.
(3)装置图中的“稀盐酸”你认为它的作用是:检验白色胶状沉淀物是Na2CO3.为了证明你的结论你觉得该添加的装置为
 (请画在上面装置图中,并请注明所需要的试剂).
(请画在上面装置图中,并请注明所需要的试剂).(4)这个实验给你体会最深的一点:相同的溶质在不同的溶剂里溶解度不同;改变传统实验采用水作溶剂的思路,反应可选择其它的溶剂(答案合理即可).
8.下列四幅坐标图分别所表示的意义不正确的是( )
| A. | 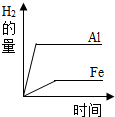 分别将等质量的铝和铁放入足量的盐酸中,放出H2的量的变化 | |
| B. | 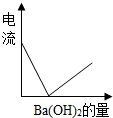 做溶液导电性实验:向一定量的硫酸铜溶液中逐滴滴入Ba(OH)2溶液至过量,则通过溶液的电流变化 | |
| C. | 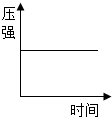 将足量的硫点燃后放入盛氧气的集气瓶中燃烧,并塞紧瓶塞,瓶内压强的变化 | |
| D. |  加热一定量氯酸钾和二氧化锰的固体混合物,二氧化锰的质量分数随加热时间的变化 |
15.呼吸面具中的“氧气再生剂”,主要成分是淡黄色固体过氧化钠(Na2O2),使用后会变成白色固体.某兴趣小组对白色固体的成分进行了探究.
【假设与猜想】根据呼出的气体中含有较多的成分与过氧化钠反应后生成的物质,作出如下猜想:
猜想一:氢氧化钠;猜想二:碳酸钠;猜想三:氢氧化钠和碳酸钠
【查阅资料】
(1)Na2CO3溶液呈碱性;CaCl2溶液呈中性.
(2)Na2O2能与水起反应生成氢氧化钠和氧气,也能与二氧化碳起反应生成碳酸钠和氧气.
【实验验证】
【讨论与反思】
同学们认为小明的实验不能得出这一结论,理由是Na2CO3溶液显碱性,也能使酚酞溶液变红.
实验步骤中第4步的反应原理,用化学方程式表示为CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
【得出结论】猜想三成立.
【拓展应用】“氧气再生剂”的保存方法是密封保存.
【假设与猜想】根据呼出的气体中含有较多的成分与过氧化钠反应后生成的物质,作出如下猜想:
猜想一:氢氧化钠;猜想二:碳酸钠;猜想三:氢氧化钠和碳酸钠
【查阅资料】
(1)Na2CO3溶液呈碱性;CaCl2溶液呈中性.
(2)Na2O2能与水起反应生成氢氧化钠和氧气,也能与二氧化碳起反应生成碳酸钠和氧气.
【实验验证】
| 实验步骤 | 实验现象[ | 结 论 |
| 1.小明同学取少量白色固体于试管中,加水溶解,然后滴加酚酞溶液. | 溶液变红色 | 白色固体中一定含有氢氧化钠. |
| 2.小红取少量白色固体于试管中,加入稀盐酸. | 出现大量气泡 | 白色固体中一定含有碳酸钠 |
| 3.小玉取少量白色固体于试管中,加水溶解,再加入足量的氯化钙溶液. | 出现白色沉淀 | |
| 4.小玉待第3步充分反应后过滤,向滤液中滴加硫酸铜溶液. | 出现蓝色沉 | 白色固体中一定含有氢氧化钠 |
同学们认为小明的实验不能得出这一结论,理由是Na2CO3溶液显碱性,也能使酚酞溶液变红.
实验步骤中第4步的反应原理,用化学方程式表示为CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
【得出结论】猜想三成立.
【拓展应用】“氧气再生剂”的保存方法是密封保存.
13.下列物质在氧气中燃烧,生成物是黑色固体的是( )
| A. | 木炭 | B. | 铁丝 | C. | 镁条 | D. | 红磷 |
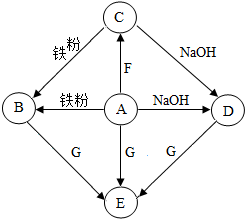 A-G是初中化学常见物质.其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.