题目内容
5.如图是一氧化碳与氧化铁反应的装置示意图.请回答下列问题:
(1)写出图中的实验现象:红色粉末变黑;澄清石灰水变浑浊.
(2)图中装置的不足之处是;没有尾气处理装置.
(3)请写出反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;CO2+Ca(OH)2═CaCO3↓+H2O.
(4)要制得含Fe96%的生铁210t,至少需要含Fe2O380%的铁矿石(杂质不含铁)多少吨?
分析 根据一氧化碳与氧化铁反应生成铁和二氧化碳,及二氧化碳的特性和方程式的书写原则解答.根据化学变化前后元素质量不变,生铁中所含铁的质量与赤铁矿石中所含铁元素质量相等,利用这一等量关系解决本问题,其中赤铁矿石中铁元素质量即铁矿石中氧化铁所含铁元素的质量.
解答 解:(1)一氧化碳与氧化铁反应生成铁和二氧化碳,氧化铁是红色粉末,铁粉是黑色,二氧化碳能使澄清的石灰水变浑浊;
故答案为:红色粉末变黑;澄清石灰水变浑浊;
(2)该实验过程为:通一氧化碳排尽试管内空气-加热-停止加热-继续通一氧化碳至试管冷却,从步骤可看出,一氧化碳并未完全进行反应,而一氧化碳与石灰水不反应,且有毒,所以要进行尾气处理,在b处添加酒精灯或进行尾气收集,而装置中没有;
故答案为:没有尾气处理装置;
(3)一氧化碳与氧化铁在高温下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;二氧化碳与氢氧化钙在常温下反应生成碳酸钙和水,反应的化学方程式为为:CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;CO2+Ca(OH)2═CaCO3↓+H2O.
(4)设需要含Fe2O380%的铁矿石质量为x
210t×96%=x×80%×$\frac{56×2}{56×2+16×3}$×100%
x=360t
答:需要含Fe2O380%的铁矿石360t.
点评 本题主要考查了一氧化碳炼铁的实验现象、方程式的书写及对装置的评价,了解相关知识是解答的关键.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
13.物理变化与化学变化的根本区别是( )
| A. | 颜色是否发生了变化 | B. | 物质的状态是否发生了变化 | ||
| C. | 物质的种类是否发生了变化 | D. | 物质的质量是否发生了变化 |
10.神舟八号飞船进人轨道后,太阳能电池帆板打开,并自动调整位置,使太阳光垂直照射在帆板上,这样就能产生足够的电能,用于各种仪器设备正常工作.这种太阳能电池帆板的作用是( )
| A. | 将太阳能转化为化学能 | B. | 将太阳能转化为电能 | ||
| C. | 将电能转化为太阳能 | D. | 将热能转化为太阳能 |
14.化学实验有助于理解化学知识,形成化学观念,提升科学素.用如图所示装置进行实验(夹持装置已省略).请完成下列内容.
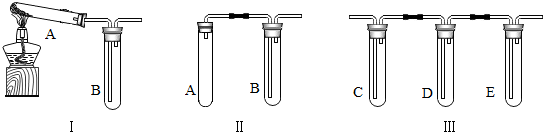
(1)制取气体.
(2)证明二氧碳能与水反应,将制CO2的装置与Ⅲ装置连接,若B中装入饱和NaHCO3溶液,则C、D、E中还应分别装入硝酸银溶液、浓硫酸、紫色石蕊试液.
(3)探究碳的还原性,将图中的Ⅰ、Ⅲ装置连接,在Ⅰ装置的A试管中加入碳和氧化铜粉末.若反应既有CO2又有CO生成,要证明CO2生成并收集CO,B、D中都加入澄清石灰水,C中加入NaOH溶液,证明有CO2生成的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,D的作用是检验二氧化碳是否被C中的氢氧化钠溶液完全吸收,E用于收集CO,应对E装置进行的调整是进气管短,出气管要长.

(1)制取气体.
| 气体 | 反应物 | 装置 | 化学方程式 |
| O2 | Ⅰ | ||
| CO2 | 石灰石、稀盐酸 |
(3)探究碳的还原性,将图中的Ⅰ、Ⅲ装置连接,在Ⅰ装置的A试管中加入碳和氧化铜粉末.若反应既有CO2又有CO生成,要证明CO2生成并收集CO,B、D中都加入澄清石灰水,C中加入NaOH溶液,证明有CO2生成的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,D的作用是检验二氧化碳是否被C中的氢氧化钠溶液完全吸收,E用于收集CO,应对E装置进行的调整是进气管短,出气管要长.
14.下列是表示气体粒子的示意图,图中“ ”和“
”和“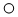 ”分别表示两种不同质子数的原子,其中可能表示氧化物的是( )
”分别表示两种不同质子数的原子,其中可能表示氧化物的是( )
 ”和“
”和“ ”分别表示两种不同质子数的原子,其中可能表示氧化物的是( )
”分别表示两种不同质子数的原子,其中可能表示氧化物的是( )
| A. | 只有①④ | B. | ②③④ | C. | 只有② | D. | ①②③④ |
 新药帕拉米韦注射液可用于治疗H7N9禽流感.其说明书中部分如图.
新药帕拉米韦注射液可用于治疗H7N9禽流感.其说明书中部分如图.