题目内容
20. 儿童缺锌会引起食欲不振、发育不良.如图是某种补锌口服液的说明书的一部分.请回答:
儿童缺锌会引起食欲不振、发育不良.如图是某种补锌口服液的说明书的一部分.请回答:(1)该口服液中的锌属于微量(填“常量”或“微量”)元素;
(2)葡萄糖酸锌中碳、氧、氢元素的质量比为72:11:112
(3)每支口服液中 锌的质量分数是0.05%
(4)在葡萄糖酸锌中,锌元素的质量分数是31.7%
(5)若儿童每1Kg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半,则体重为40Kg的儿童每天还须服该口服液几支才能满足身体的需要.
分析 (1)根据已有的知识进行分析,锌属于人体所需的微量元素;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
(3)根据标签信息来分析;
(4)根据化合物中元素质量分数度的计算方法来分析;
(5)体重为40kg的儿童每天需要锌0.5mg×40=20mg,其中一半即10mg由口服液提供,由此判断该儿童每天须服口服液的量.
解答 解:(1)锌属于人体所需的微量元素,故填:微量;
(2)葡萄糖酸锌中碳、氧、氢元素的质量比为(12×12):(1×22):(16×14)=72:11:112;故填:72:11:112;
(3)由标签可知,每支口服液含锌5.0mg,则每支口服液中锌的质量分数=$\frac{5.0mg}{10.0×1000mg}×100%$=0.05%;故答案为:0.05%;
(4)葡萄糖酸锌中碳元素的质量分数=$\frac{65}{(12×12)+(1×22)+(16×14)+65}×100%$=31.7%;故填:31.7%;
(5)儿童1kg体重每日需要0.5mg锌,体重为40kg的儿童每日需要锌=0.5mg×$\frac{40kg}{1kg}$=20mg;其中一半由口服液提供,则每日需要通过该口服液补充锌1mg;根据标签可知,每支口服液含锌为5mg,所以该儿童每天还须服该口服液2支;
故答案为:2.
点评 由标签获得重要信息如物质的化学式、组成成分、各成分的含量等等是解决标签类问题的基础.

练习册系列答案
相关题目
11.关于氮气、一氧化二氮、五氧化二氮这三种物质的叙述中,正确的是( )
| A. | 都含有氮分子 | B. | 组成三种物质的元素种类相同 | ||
| C. | 在一个分子中所含的氮原子数相同 | D. | 各物质中氮元素的质量分数相同 |
8.“绿色化学”的核心是在化学反应过程或化工生产中,尽量减少使用或彻底消除有害物质.下列做法中,符合绿色化学的是( )
| A. | 生产和使用剧毒农药 | B. | 用二氧化硫漂泊纸浆 | ||
| C. | 化工厂产生的废气向高空排放 | D. | 利用双氧水制氧气 |
12.下列微粒结构示意图中,表示阳离子的是( )
| A. | 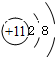 | B. | 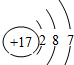 | C. | 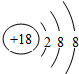 | D. | 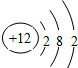 |
10.下列关于实验现象的描述,正确的是( )
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 硫在空气中燃烧发出蓝紫色火焰 | |
| C. | 铁在空气中剧烈燃烧,火星四射 | |
| D. | 电解水时正极与负极产生的气体体积比为1:2 |
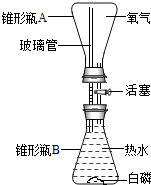 如图是为探究物质燃烧条件设计的实验(热水的温度超过白磷着火点).请写出磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
如图是为探究物质燃烧条件设计的实验(热水的温度超过白磷着火点).请写出磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.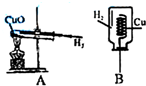 实验是进行科学探究的重要途径.在探究过程中,很多因素都会对实验结果产生影响.
实验是进行科学探究的重要途径.在探究过程中,很多因素都会对实验结果产生影响.