题目内容
4.测空气中的氧气体积占比的实验中,止水夹松动,测试结果偏大还是偏小.为什么.分析 根据测量空气中氧气含量时止水夹未加紧,实验中逸出了一部分气体,最终进入瓶内的水增多分析解答.
解答 解:
测量空气中氧气含量时,若止水夹没有夹紧,则在压强差的作用下,导管口有气泡冒出;因实验中逸出了一部分气体,所以最终进入瓶内的水增多,导致测量结果偏大.
故答案为:
偏大;因实验中逸出了一部分气体,所以最终进入瓶内的水增多.
点评 掌握测定空气中氧气体积分数的注意事项,此题属于基础知识题,难度较小.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
15.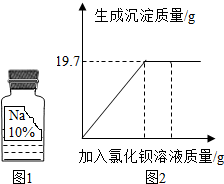 实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,该瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.CaCl2溶液和BaCl2溶液都呈中性.
Ⅱ.初中化学中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3,其中一种物质的类别有别于其它三种物质,该物质是氢氧化钠或NaOH.
Ⅲ.室温(20℃)时,四种物质的溶解度数据如下:
【资料分析】依据上述资料分析该瓶试剂也不可能是碳酸氢钠或NaHCO3.
【实验探究】
实验1:实验测得该溶液的pH>7,则这瓶试剂也不可能是氯化钠或NaCl.
实验2:为了检验该溶液是NaOH溶液还是Na2CO3溶液,又进行了如下实验:
取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.写出上述反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
实验3:有同学对实验2结论提出质疑,认为该溶液可能是部分变质的氢氧化钠溶液,请你设计实验来验证.写出实验步骤、现象和结论.
【计算】取试剂瓶中的溶液50g,逐滴加入一定溶质质量分数的BaCl2溶液.实验过程中,生成沉淀质量与加入BaCl2溶液的质量关系如图2所示,试计算溶液中碳酸钠的质量分数.
 实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.
实验室里有一瓶保管不当、标签残缺的试剂瓶,标签中只剩下“Na”和“10%”字样(如图1所示),某兴趣小组对其组成进行如下探究.【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,该瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.CaCl2溶液和BaCl2溶液都呈中性.
Ⅱ.初中化学中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3,其中一种物质的类别有别于其它三种物质,该物质是氢氧化钠或NaOH.
Ⅲ.室温(20℃)时,四种物质的溶解度数据如下:
| 物质 | NaHCO3 | NaCl | NaOH | Na2CO3 |
| 溶解度g/100g水 | 9.6 | 36 | 109 | 215 |
【实验探究】
实验1:实验测得该溶液的pH>7,则这瓶试剂也不可能是氯化钠或NaCl.
实验2:为了检验该溶液是NaOH溶液还是Na2CO3溶液,又进行了如下实验:
取少量溶液于试管中,滴加足量的盐酸,有气泡产生,得出结论,该溶液是Na2CO3溶液.写出上述反应的化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
实验3:有同学对实验2结论提出质疑,认为该溶液可能是部分变质的氢氧化钠溶液,请你设计实验来验证.写出实验步骤、现象和结论.
【计算】取试剂瓶中的溶液50g,逐滴加入一定溶质质量分数的BaCl2溶液.实验过程中,生成沉淀质量与加入BaCl2溶液的质量关系如图2所示,试计算溶液中碳酸钠的质量分数.
9.推理是化学学习的一种重要思维方法,以下推理合理的是( )
| A. | 一氧化碳和二氧化碳两种物质的组成元素相同,所以它们的化学性质相同 | |
| B. | 活泼金属与稀盐酸反应放出气体,所以与稀盐酸反应放出气体的物质一定是活泼金属 | |
| C. | 某物质充分燃烧生成二氧化碳和水,所以该物质的组成里一定含有碳、氢两种元素 | |
| D. | 酸与碱发生中和反应时有热量放出,所以有热量放出的反应一定是中和反应 |
16.规范的操作是实验成功的前提,下列实验操作正确的是( )
| A. | 实验完毕后,实验过程中剩余的试剂都应该放回原试剂瓶 | |
| B. | 蒸发饱和食盐水,蒸发皿必须放在石棉网上,用酒精灯的外焰加热 | |
| C. | 没有腐蚀性的药品可直接放在电子秤上称量,有腐蚀性的应放在烧杯中称量 | |
| D. | 玻璃管与胶皮管连接时,将玻璃管一端用水润湿,稍用力转动插入胶皮管中 |
8.下列说法中不正确的是( )
| A. | 食用加碘食盐可以预防大脖子病 | B. | 浓硫酸溶于水能放出大量的热 | ||
| C. | 氢氧化钙可作补钙剂 | D. | 厨房洗涤剂有溶解油污的作用 |