题目内容
测得煅烧一段时间后的石灰石(成分为碳酸钙和氧化钙及20%的不含钙的杂质)中的钙元素的质量分数为50%,某同学取100克该石灰石样品继续煅烧充分反应后,产生二氧化碳的质量为( )
|
| A. | 10g | B. | 20g | C. | 30g | D. | 40g |
| 质量守恒定律及其应用;化合物中某元素的质量计算;混合物中某元素的质量计算. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | 由石灰石的质量、钙元素的质量分数为50%,可计算出石灰石中钙元素的质量,进而由质量守恒定律,反应前后钙元素的质量不变,可计算出反应后氧化钙的质量;生成二氧化碳气体的质量为石灰石的质量﹣氧化钙的质量﹣杂质的质量,据此进行分析解答. |
| 解答: | 解;测得煅烧一段时间后的石灰石(成分为碳酸钙和氧化钙及20%的不含钙的杂质)中的钙元素的质量分数为50%,100克该石灰石样品中含钙元素的质量为100g×50%=50g;由质量守恒定律,反应前后钙元素的质量不变,反应后得到氧化钙的质量为50g÷( 产生二氧化碳的质量为100g﹣70g﹣100g×20%=10g. 故选:A. |
| 点评: | 本题难度不是很大,掌握反应前后钙元素的质量不变,灵活运用质量守恒定律、化学式的有关计算是正确解答本题的关键. |

 金钥匙试卷系列答案
金钥匙试卷系列答案下列化学方程式书写正确的是( )
|
| A. | 4Al+3O2═2Al2O3 | B. | Fe+ZnSO4═FeSO4+Zn |
|
| C. | Cu2(OH)2CO3═2Cu+H2O+CO2↑ | D. | 2NaOH+CuSO4═Cu(OH)2+Na2SO4 |
对下列事实的解释正确的是( )
| 选项 | 事实 | 解释 |
| A | 很多宝石绚丽多彩 | 宝石中含有某些金属原子 |
| B | 一氧化碳使人中毒 | 一氧化碳分子有毒 |
| C | 浓硫酸有吸水性而稀硫酸没有 | 溶质的分子构成不同 |
| D | 氯化钠固体不导电 | 氯化钠固体中没有离子 |
A. A B. B C. C D. D
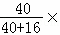 100%)=70g;
100%)=70g; 根据下列粒子结构示意图,回答问题:
根据下列粒子结构示意图,回答问题:


 (1)图中X= ,该原子的元素符号是 。 +X 2 8 1
(1)图中X= ,该原子的元素符号是 。 +X 2 8 1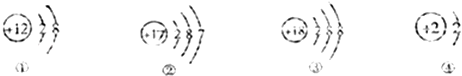


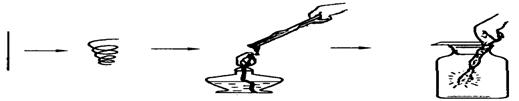
 绣,应用 进行处理,这个变化属于 变化。
绣,应用 进行处理,这个变化属于 变化。 。
。