题目内容
13.溶液与我们的生活息息相关.下列说法不正确的是( )| A. | 配制5%的硫酸溶液的一般步骤是计算、量取和稀释 | |
| B. | 氢氧化钠溶液能导电是由于溶液中含有钠离子和氢氧根离子 | |
| C. | 20℃时NaCl饱和溶液的溶质质量分数为26.5%,则该温度下NaCl的溶解度为36.1g | |
| D. | 消除路面上的积雪可以撒些盐,这样可以使雪较快地融化 |
分析 A、根据配制5%的硫酸溶液的一般步骤,进行分析判断.
B、物质的水溶液能够导电,应能产生自由移动离子,据此进行分析判断.
C、根据饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}×$100%,进行分析判断.
D、根据盐溶于水后形成盐溶液,使凝固点降低,从而加快冰雪的溶解,进行分析判断.
解答 解:A、配制5%的硫酸溶液,采用的是稀释浓硫酸的方法,一般步骤为计算、量取(浓硫酸和水)和稀释,故选项说法正确.
B、氢氧化钠溶液能导电是由于溶液中含有能自由移动的钠离子和氢氧根离子,故选项说法错误.
C、20℃时NaCl饱和溶液的溶质质量分数为26.5%,设则该温度下NaCl的溶解度为S,则$\frac{S}{S+100g}×$100%=26.5%,S≈36.1g,故选项说法正确.
D、消除路面上的积雪可以撒些盐,盐溶于水后形成盐溶液,使凝固点降低,从而加快冰雪的溶解,故选项说法正确.
故选:B.
点评 本题难度不大,掌握配制溶质质量分数一定溶液的实验步骤、溶液导电的原因、饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}×$100%等是正确解答本题的关键.

练习册系列答案
相关题目
4.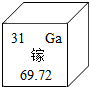 砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.无法获取到的信息是( )
砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.无法获取到的信息是( )
 砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.无法获取到的信息是( )
砷化镓(GaAs)是一种“LED”绿色节能光源材料,镓元素的相关信息如图.无法获取到的信息是( )| A. | 原子的核电荷数和最外层电子数 | B. | 元素符号和相对原子质量 | ||
| C. | 元素种类和核外电子数 | D. | 核内中子数和原子的实际质量 |
1.比较、类推是学习中常用的思维方法.现有以下类推结果中正确的是( )
| A. | 碳酸钠、碳酸钙能与稀盐酸反应,所以所有的碳酸盐都可以与稀盐酸反应 | |
| B. | 碱的水溶液显碱性,所以碱性溶液一定是碱溶液 | |
| C. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| D. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
5.下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
| A. | 氢氧化铜和稀硫酸 | B. | 氢氧化钠和稀盐酸 | ||
| C. | 氢氧化钙溶液和少量二氧化碳 | D. | 氢氧化钾和硝酸钠 |