题目内容
下列有关水的说法中正确的是( )
A. 水电解所生成氢气和氧气的质量比为2:1
B. 水沸腾时可冲起壶盖,说明温度升高分子会变大
C. 水和冰块混合得到混合物
D. 硬水是指含有较多可溶性钙、镁化合物的水
 D
【解析】A、电解水产生的氢气和氧气的体积比为2:1,而不是质量比,故错误;
B、水烧开后易把壶盖冲起,说明温度升高,分子间的间隔会变大,水分子本身不变,故错误;
C、冰块是固态的水,混合以后还是只有水这一种物质,属于纯净物,故错误;
D、硬水是指含有较多钙镁离子的水,故正确。
D
【解析】A、电解水产生的氢气和氧气的体积比为2:1,而不是质量比,故错误;
B、水烧开后易把壶盖冲起,说明温度升高,分子间的间隔会变大,水分子本身不变,故错误;
C、冰块是固态的水,混合以后还是只有水这一种物质,属于纯净物,故错误;
D、硬水是指含有较多钙镁离子的水,故正确。
 阅读快车系列答案
阅读快车系列答案某学生要称量




A. 所量水的实际体积小于
B. 称得氯化钠的实际质量小于
C. 配得溶液的实际质量可能大于

D. 若砝码表面有少量锈斑(仍放左盘),则称得的氯化钠实际质量一定小于或等于
 BC
【解析】
根据读数时必须平时,使眼、刻度和液面的最低点三点共线,可知仰视时液体的最低点偏上,即量取的水的体积大于94.4毫升,A选项错误;称量5.6g克氯化钠的操作是取砝码5g,游码移到0.6g处,然后加氯化钠使天平平衡,题中将砝码放反了,所称氯化钠的质量为5g-0.6g=4.4g,B选项正确;根据选项A知溶剂水的质量增大,根据选项B知溶质氯化钠的质量偏小,所以二者的质量之和的变...
BC
【解析】
根据读数时必须平时,使眼、刻度和液面的最低点三点共线,可知仰视时液体的最低点偏上,即量取的水的体积大于94.4毫升,A选项错误;称量5.6g克氯化钠的操作是取砝码5g,游码移到0.6g处,然后加氯化钠使天平平衡,题中将砝码放反了,所称氯化钠的质量为5g-0.6g=4.4g,B选项正确;根据选项A知溶剂水的质量增大,根据选项B知溶质氯化钠的质量偏小,所以二者的质量之和的变... 根据化学实验操作规则,请用适当的数据填空:
(1)向酒精灯里添加酒精,不可超过酒精灯容积的_____。
(2)给试管里的液体加热,液体体积不超过试管容积的______;试管口斜向上,且与桌面成_____角。
(3)取用液体药品时,若没有说明用量,一般取_________mL。
(4)洗涤试管时,先倒净试管内的废液,再注入约_____体积的水。
 三分之二三分之一45度1至2试管容积一半
【解析】
(1)向酒精灯里添加酒精,不可超过酒精灯容积的三分之二,不少于酒精灯容积的三分之一;
(2)给试管里的液体加热,液体体积不超过试管容积的三分之一,防止液体沸腾飞溅出来;试管口斜向上,且与桌面成45度角;
(3)取用液体药品时,若没有说明用量,以节约药品为原则,一般取1至2mL;
(4)洗涤试管时,先倒净试管内的废液,...
三分之二三分之一45度1至2试管容积一半
【解析】
(1)向酒精灯里添加酒精,不可超过酒精灯容积的三分之二,不少于酒精灯容积的三分之一;
(2)给试管里的液体加热,液体体积不超过试管容积的三分之一,防止液体沸腾飞溅出来;试管口斜向上,且与桌面成45度角;
(3)取用液体药品时,若没有说明用量,以节约药品为原则,一般取1至2mL;
(4)洗涤试管时,先倒净试管内的废液,... 图A所示是用红磷在空气中燃烧的方法测定空气中氧气含量.(在集气瓶中装入少许水,会使生成的五氧化二磷烟状物迅速溶解).

(1)实验原理:①红磷在空气中燃烧反应的符号表达式 ____________ .
②密闭的装置内,由于 ______ 被消耗,生成固体物质,该装置内气体压强 ______ .
(2)实验探究:
第一步:集气瓶装入少许水,然后将集气瓶空的容积划分为五等份,并做好标记.
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的 .
.
(3)实验结论:①空气中氧气约占空气总体积的 ______ ②该实验证明了氧气具有 ______ 的性质.同时也证明了氮气有哪些性质? ______ (写一点)
(4)反思与评价:①实验完毕,若进入集气瓶中水的体积不到总容积的 ,你认为导致这一结果的原因可能是 ______ .(写一点)
,你认为导致这一结果的原因可能是 ______ .(写一点)
②某同学对实验进行反思后,提出了改进方法(如图B所示),你认为改进后的优点是___________ .
(5)拓展迁移:已知:镁在氧气中燃烧生成氧化镁,镁在氮气中燃烧生成氮化镁(固体),能否用镁代替红磷测定空气中氧气的含量?并简要说明理由. 答: ______ (填“能”或“不能”),理由 ____________ .
 P+O2 P2O5氧气减小1/5 支持燃烧不燃烧,也不支持燃烧,(或难溶于水 )红磷量不足;或装置漏气;或未等冷却至室温打开止水夹装置始终密封,空气没有逸出,实验结果准确不能镁燃烧不仅能跟氧气反应,还能跟氮气反应,水面上升超过1/5 ,无法证明空中氧气的含量。
【解析】
(1)实验原理:①符号表达式的书写:将反应物的符号写在箭头的左侧,生成物的符号写在箭头的右侧,在箭头的上方或下方注明...
P+O2 P2O5氧气减小1/5 支持燃烧不燃烧,也不支持燃烧,(或难溶于水 )红磷量不足;或装置漏气;或未等冷却至室温打开止水夹装置始终密封,空气没有逸出,实验结果准确不能镁燃烧不仅能跟氧气反应,还能跟氮气反应,水面上升超过1/5 ,无法证明空中氧气的含量。
【解析】
(1)实验原理:①符号表达式的书写:将反应物的符号写在箭头的左侧,生成物的符号写在箭头的右侧,在箭头的上方或下方注明... 如图装置可用于测定空气中氧气的含量。下列说法不正确的是
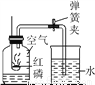
A. 实验时红磷一定要过量
B. 该实验证明氧气约占空气总体积的
C. 通过该实验还可以了解氮气的一些性质
D. 红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹
 D
【解析】A、红磷要足量,保证氧气消耗完,测量结果和准确,正确;B、本实验的结论是:氧气约占空气总体积的五分之一,正确;C、通过该实验还可以了解氮气既不能燃烧,也不能支持燃烧;氮气难溶于水等,正确;D、冒出大量的白烟,不是白雾,应使装置冷却后再打开弹簧夹并观察水面变化情况,错误;故选D。
D
【解析】A、红磷要足量,保证氧气消耗完,测量结果和准确,正确;B、本实验的结论是:氧气约占空气总体积的五分之一,正确;C、通过该实验还可以了解氮气既不能燃烧,也不能支持燃烧;氮气难溶于水等,正确;D、冒出大量的白烟,不是白雾,应使装置冷却后再打开弹簧夹并观察水面变化情况,错误;故选D。 某班同学用氢氧化钠溶液和稀盐酸进行中和反应实验:
(1)甲同学在烧杯中加入约5 mL氢氧化钠溶液,滴入几滴__________溶液,此时溶液呈红色,接着用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液变为无色,于是他得出两者恰好中和的结论,反应的化学方程式为_______________________________。
(2)乙同学对甲同学的结论提出了质疑,并对反应后溶液中的溶质成分进行探究。
(实验探究)反应后溶液中的溶质是什么?
猜想一:只有NaCl 猜想二:____________ 猜想三:NaCl和NaOH
以上猜想中,你觉得不合理的是________。
为了验证另外两种猜想,乙同学设计如下实验方案:
实验操作 | 实验现象 | 实验结论 |
取少量反应后的溶液于试管中滴入Na2CO3溶液 | ________ | 猜想二成立 |
(反思交流)实验结束后,废液处理方法正确的是________(填序号)。
A. 倒入下水道 B. 倒入废液缸 C. 带出实验室
 无色酚酞NaOH+HCl=== NaCl+H2ONaCl和HCl猜想三有气泡产生B
【解析】
本题主要考查中和反应及其应用,实验探究物质的组成成分以及含量。可根据氢氧化钠和盐酸反应生成了氯化钠和水写出反应的方程式;【猜想】根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余;【进行实验】根据酚酞遇碱变红来进行解答;根据实验的结论进行发生反思。
(1)氢氧化钠溶液呈...
无色酚酞NaOH+HCl=== NaCl+H2ONaCl和HCl猜想三有气泡产生B
【解析】
本题主要考查中和反应及其应用,实验探究物质的组成成分以及含量。可根据氢氧化钠和盐酸反应生成了氯化钠和水写出反应的方程式;【猜想】根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余;【进行实验】根据酚酞遇碱变红来进行解答;根据实验的结论进行发生反思。
(1)氢氧化钠溶液呈... 用化学用语填空:
(1)2个氢原子_____;
(2)2个亚铁离子_____;
(3)标注高锰酸钾中锰元素的化合价_____;
(4)已知次氯酸钠的化学式为NaClO,试写出次氯酸钙的化学式_____。
 2H; 2Fe2+; KO4; Ca(ClO)2。
【解析】
(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氢原子表示为2H;
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其元素符号前加上相应的数字,故2个亚铁离子可...
2H; 2Fe2+; KO4; Ca(ClO)2。
【解析】
(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氢原子表示为2H;
(2)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其元素符号前加上相应的数字,故2个亚铁离子可... 为测定空气中氧气的含量,小华和小强同学分别设计如下方案: 小华:采用图 1 装置进行实验(燃烧匙中药品为红磷)
小强:(如图 2)选用实际容积为 40mL 的试管作反应容器,将过量的自磷放入试管,用橡皮 塞塞紧试管,通过导管与实际容积为 60mL 且润滑性很好的针筒注射器组成如下图的实验装 置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不 计,请回答下列问题:

(1)红磷在集气瓶中燃烧的现象是_________________________ ,冷却到室温打开止水夹后 的现象______________________ ,红磷燃烧的文字表达___________________________ ;
(2)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到进入集气瓶中水的体积不到总 容积的 1/5,你认为其原因可能是_______________,______________________ ;
(3)如果将燃烧匙中红磷换成硫粉,实验能否成功?为什么?_____________
(4)实验前,打开弹簧夹,将注射器活塞前沿从 20mL 刻度处推至 15mL 刻度处,然后松开手,若活塞仍能返回至 20mL 刻度处,则说明_____;若先夹紧弹簧夹, 用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹,可观察到的现象是_____; 若不夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹,可观察到 的现象为_____
(5)图 2 的设计操作与图 1 比较,其优点是_____
(6)若按小强的设想进行实验,实际可能遇到诸多问题而发生危险,造成实验失败,例如:_____、_____、_____等。
 发出黄白色火焰,放热,产生大量白烟产生大量白烟烧杯中的水进入集气瓶,占集气瓶上方空气体积的 1/5 左右磷+氧气五氧化二磷红磷的量不足装置漏气(未等装置冷却就打开弹簧机)不能,硫磺燃烧产生二氧化硫是气体,影响气压装置气密性良好注射器向左移动到12mL处停止先向右移动,再向左移动到8mL处停止减少空气污染,结果更准确橡胶塞弹出试管炸裂注射器活塞弹出来等
【解析】
(1)红磷在集气瓶中燃烧...
发出黄白色火焰,放热,产生大量白烟产生大量白烟烧杯中的水进入集气瓶,占集气瓶上方空气体积的 1/5 左右磷+氧气五氧化二磷红磷的量不足装置漏气(未等装置冷却就打开弹簧机)不能,硫磺燃烧产生二氧化硫是气体,影响气压装置气密性良好注射器向左移动到12mL处停止先向右移动,再向左移动到8mL处停止减少空气污染,结果更准确橡胶塞弹出试管炸裂注射器活塞弹出来等
【解析】
(1)红磷在集气瓶中燃烧... 某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出铁丝在氧气中燃烧的文字表达式:_______。已知铁丝燃烧生成四氧化三铁。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?

点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。
由此可知:蜡烛燃烧产生的火焰是由_______(填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其_______(填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时,__________(填“有”或“没有”)火焰产生。
(4)木炭在氧气中燃烧没有火焰,其原因可能是_________ 。
 铁+氧气四氧化三铁气态;沸点有木炭燃烧的过程中产生了可燃性的气体继续燃烧产生的火焰。
【解析】
(1)铁与氧气在点燃的条件下反应生成四氧化三铁,反应的文字表达式为铁+氧气四氧化三铁;
(2)由题可知,金属导管的另一端也能燃烧,说明蜡烛燃烧产生的火焰是由气态物质燃烧形成的;
(3)可燃物变成气体的才会形成火焰,如果反应的温度不能使可燃物气化,则不会有火焰产生,而只能在液体或固...
铁+氧气四氧化三铁气态;沸点有木炭燃烧的过程中产生了可燃性的气体继续燃烧产生的火焰。
【解析】
(1)铁与氧气在点燃的条件下反应生成四氧化三铁,反应的文字表达式为铁+氧气四氧化三铁;
(2)由题可知,金属导管的另一端也能燃烧,说明蜡烛燃烧产生的火焰是由气态物质燃烧形成的;
(3)可燃物变成气体的才会形成火焰,如果反应的温度不能使可燃物气化,则不会有火焰产生,而只能在液体或固... 
