题目内容
实验室使用下列所示装置制备、收集和检验气体.请回答下列问题:(需要填装置图的应选填相应的序号)(1)写出图中标号的仪器名称:①______,②______.
(2)利用装置A可制得的气体的化学方程式是______△2KCl+3O2↑
【答案】分析:(1)依据常用仪器回答;
(2)装置A适用于加热固体制取气体,实验室用氯酸钾和二氧化锰混合加热制取氧气符合此条件,据反应原理书写方程式;并依据实验室制取氢气的反应物的状态、反应条件选择发生装置,据气体的密度和溶解性选择收集装置;
(3)依据发生装置的选择方法进行判断;依据反应原理书写方程式;检验二氧化碳用澄清的石灰水,并依据二氧化碳的性质选择收集装置;
(4)依据发生装置的选择方法并结合题意进行分析.
解答:解:(1)标号仪器分别是长颈漏斗和集气瓶;
(2)装置A适用于加热固体制取气体,实验室用氯酸钾和二氧化锰混合加热制取氧气符合此条件,该装置试管口没有棉花,所以高锰酸钾制取氧气不适合用此装置,氯酸钾制取氧气反应的方程式是:2KClO3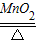 2KCl+3O2↑;实验室制取氢气是用锌与稀硫酸常温反应制取,故选发生装置B,氢气密度比空气小且难溶于水,可用向下排空气法或排水法收集,图示无向下排空气法,故选C;
2KCl+3O2↑;实验室制取氢气是用锌与稀硫酸常温反应制取,故选发生装置B,氢气密度比空气小且难溶于水,可用向下排空气法或排水法收集,图示无向下排空气法,故选C;
(3)实验室制取二氧化碳用大理石与稀盐酸反应制取,不需加热,故选B发生装置,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;检验二氧化碳用澄清的石灰水,二氧化碳密度比空气大且能溶于水,故只能用向上排空气法收集;
(4)由题意可知,制取氯气要用到浓盐酸,是液体,故不能用A装置,试管口向下会导致液体流出;且该反应需要加热,所以也不能用B装置;
故答案为:
(1)长颈漏斗;集气瓶;
(2)2KClO3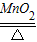 2KCl+3O2↑;BC;
2KCl+3O2↑;BC;
(3)B;CaCO3+2HCl=CaCl2+H2O+CO2↑;D;E;
(4)①不可以,浓盐酸是液体;②不可以,反应需要加热.
点评:本题主要考查了对发生和收集装置选取方法的掌握和应用,及正确书写化学方程式的能力,能较好考查学生分析、解决问题的能力.
(2)装置A适用于加热固体制取气体,实验室用氯酸钾和二氧化锰混合加热制取氧气符合此条件,据反应原理书写方程式;并依据实验室制取氢气的反应物的状态、反应条件选择发生装置,据气体的密度和溶解性选择收集装置;
(3)依据发生装置的选择方法进行判断;依据反应原理书写方程式;检验二氧化碳用澄清的石灰水,并依据二氧化碳的性质选择收集装置;
(4)依据发生装置的选择方法并结合题意进行分析.
解答:解:(1)标号仪器分别是长颈漏斗和集气瓶;
(2)装置A适用于加热固体制取气体,实验室用氯酸钾和二氧化锰混合加热制取氧气符合此条件,该装置试管口没有棉花,所以高锰酸钾制取氧气不适合用此装置,氯酸钾制取氧气反应的方程式是:2KClO3
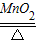 2KCl+3O2↑;实验室制取氢气是用锌与稀硫酸常温反应制取,故选发生装置B,氢气密度比空气小且难溶于水,可用向下排空气法或排水法收集,图示无向下排空气法,故选C;
2KCl+3O2↑;实验室制取氢气是用锌与稀硫酸常温反应制取,故选发生装置B,氢气密度比空气小且难溶于水,可用向下排空气法或排水法收集,图示无向下排空气法,故选C;(3)实验室制取二氧化碳用大理石与稀盐酸反应制取,不需加热,故选B发生装置,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;检验二氧化碳用澄清的石灰水,二氧化碳密度比空气大且能溶于水,故只能用向上排空气法收集;
(4)由题意可知,制取氯气要用到浓盐酸,是液体,故不能用A装置,试管口向下会导致液体流出;且该反应需要加热,所以也不能用B装置;
故答案为:
(1)长颈漏斗;集气瓶;
(2)2KClO3
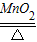 2KCl+3O2↑;BC;
2KCl+3O2↑;BC;(3)B;CaCO3+2HCl=CaCl2+H2O+CO2↑;D;E;
(4)①不可以,浓盐酸是液体;②不可以,反应需要加热.
点评:本题主要考查了对发生和收集装置选取方法的掌握和应用,及正确书写化学方程式的能力,能较好考查学生分析、解决问题的能力.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
常温下,铁与水几乎不反应,但高温下,铁能与水蒸气反应,生成四氧化三铁(磁铁矿的主要成分)和氢气.请设计实验,证明铁粉与水蒸气能够发生反应并且产生了氢气.
(1)铁粉与水蒸气反应的化学方程式是: ,该反应的基本反应类型是 .
(2)某兴趣小组同学用如图所示装置进行实验(D可以重复利用),请你协助该小组同学完成以下实验:①实验结束后,发现B中铁粉全部转化产生了黑色块状固体,为了证明黑色固体不是铁粉,该兴趣小组同学取黑色固体进行实验,请你帮他们完成下列实验报告:
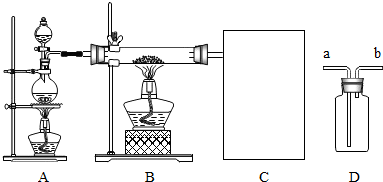
②为了除去B中出来的水蒸气,该小组同学在C中首先连接了D作为洗气装置对氢气进行干燥,则D瓶中填装的药品可以是 ;
③为了收集和验证所产生的氢气,该小组同学使用D作为气体的收集装置,则气体应该从 (填“a”或“b”)通入.
④实验室通常用浓盐酸与二氧化锰共热的方法来制取氯气,一般可选用装置A做气体的发生装置,理由是 .
(1)铁粉与水蒸气反应的化学方程式是:
(2)某兴趣小组同学用如图所示装置进行实验(D可以重复利用),请你协助该小组同学完成以下实验:①实验结束后,发现B中铁粉全部转化产生了黑色块状固体,为了证明黑色固体不是铁粉,该兴趣小组同学取黑色固体进行实验,请你帮他们完成下列实验报告:

| 实验操作 | 实验现象 | 实验结论 |
| 黑色固体不是铁粉 |
③为了收集和验证所产生的氢气,该小组同学使用D作为气体的收集装置,则气体应该从
④实验室通常用浓盐酸与二氧化锰共热的方法来制取氯气,一般可选用装置A做气体的发生装置,理由是