题目内容
7.下列关于铁的叙述不正确的是( )| A. | 纯铁为银白色金属 | B. | 纯铁有良好的延展性 | ||
| C. | 铁丝在氧气中可以燃烧 | D. | 铁跟稀硫酸反应生成硫酸铁 |
分析 根据铁是一种有银白色光泽的金属,纯铁较软,有良好的延展性,是电和热的导体,铁和氧气在点燃的条件下生成四氧化三铁,铁和稀硫酸反应生成硫酸亚铁和氢气进行分析.
解答 解:A、纯铁是银白色的金属,故A正确;
B、纯铁具有良好的延展性,故B正确;
C、铁和氧气在点燃的条件下生成四氧化三铁,故C正确;
D、铁和稀硫酸反应生成硫酸亚铁和氢气,故D错误.
故选:D.
点评 熟练掌握有关铁的性质,通过题目对铁的有关知识进行归纳总结,掌握基础知识点即可轻松解题.

练习册系列答案
相关题目
17.如图,是A、B两种物质的溶解度曲线.下列说法正确的是( )
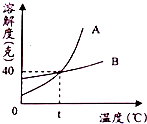

| A. | t℃时A物质饱和溶液的溶质质量分数为40% | |
| B. | B物质的溶解度受温度的影响比A物质大 | |
| C. | t℃时B物质饱和溶液降温后仍然饱和 | |
| D. | A物质的溶解度大于B物质 |
2.将25克蓝矾(CuSO4•5H2O)溶于100克水中,所得溶液中溶质的质量分数是( )
| A. | 25% | B. | 20% | C. | 12.8% | D. | 6.4% |
12.某样品为铁粉和铜粉的混合物,为了测定样品中含铜的质量分数,甲、乙、丙、丁四同学用同一样品分别进行实验.测得数据如下:
分析实验数据,回答以下问题:
(1)样品中铜的质量分数是多少?
(2)乙同学反应后的溶液质量是多少?
| 甲 | 乙 | 丙 | 丁 | |
| 所取固体样品的质量(g) | 20 | 15 | 10 | 10 |
| 加入硫酸溶液的质量(g) | 100 | 100 | 100 | 120 |
| 反应后剩余固体质量(g) | 14.4 | 9.4 | 4.4 | 4.4 |
(1)样品中铜的质量分数是多少?
(2)乙同学反应后的溶液质量是多少?
19.下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是( )
| A. | NaOH溶液中混有Ba(OH)2(K2SO4) | B. | CO2中混有HCl气体(NaOH溶液) | ||
| C. | CO2中混有CO(炽热的炭) | D. | Cu(NO3)2溶液中混有AgNO3(Cu粉) |
16.今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、Ba2+、Cl-、SO42-、CO32-.现取200ml溶液加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g.根据上述实验,以下对混合物的水溶液说法正确的是( )
| A. | 一定含SO42-和Na+,一定不含Ba2+和CO32-,可能含Cl- | |
| B. | 一定含CO32-和SO42-,一定不含Ba2+和Na+,可能含Cl- | |
| C. | 一定含CO32-、SO42-和Na+,一定不含Ba2+,可能含Cl- | |
| D. | 一定含CO32-和SO42-,一定不含Ba2+,可能含Cl-和Na+ |
17.下列哪项能证明烧杯中的硝酸钾溶液是饱和溶液( )
| A. | 将液体降温时,杯底能析出固体 | |
| B. | 蒸发水分时,杯底能析出固体 | |
| C. | 将液体倒出一部分,仍不能析出固体 | |
| D. | 加入少量硝酸钾,发现一点儿都不能再继续溶解 |