题目内容
已知铜锈的主要成分是碱式碳酸铜化学式为[Cu2(OH)2CO3],则该物质中 元素的质量分数最大,各元素原子的个数比是 .
考点:化学式的书写及意义,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:根据物质中各元素的质量比来比较元素质量分数的大小,根据化学式来分析原子个数比.
解答:解:碱式碳酸铜中的铜、氧、氢、碳四种元素的质量比是(64×2):(16×5):(1×2):12=64:40:1:6.可见其中铜元素的质量分数最大;由铜绿的化学式可知,1个铜绿分子是由2个铜原子、2个氢原子、1个碳原子和5个氧原子构成的,铜绿中原子个数比:Cu:O:H:C=2:5:2:1.
故答案为:
铜(或Cu);Cu:O:H:C=2:5:2:1
故答案为:
铜(或Cu);Cu:O:H:C=2:5:2:1
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
下列物质中,属于纯净物的是( )
| A、空气 | B、石油 |
| C、生铁 | D、二氧化碳 |
 (1)小明同学课下自制了如图的实验装置,对水通电分解进行了实验探究,请你和他一起完成此实验.
(1)小明同学课下自制了如图的实验装置,对水通电分解进行了实验探究,请你和他一起完成此实验.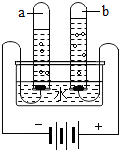 如图所示是电解水的实验装置图,请回答:
如图所示是电解水的实验装置图,请回答: