题目内容
7.水是生命的源泉,下列变化与水相关.请回答:①二氧化碳溶于水发生反应的化学方程式是CO2+H2O=H2CO3.
②自来水厂净水过程中常用到活性炭,其作用是吸附作用.
③铁丝在氧气中燃烧时,集气瓶内放少量水的目的是防止溅落的熔化物炸裂瓶底.
④除去粗盐中泥沙等难溶性杂质的实验步骤:
I.操作a的名称是过滤.
II.三个步骤都用到的玻璃仪器是玻璃棒.
⑤甲和乙两种固体物质(不含结晶水)的溶解度曲线如图1所示,回答下列问题:
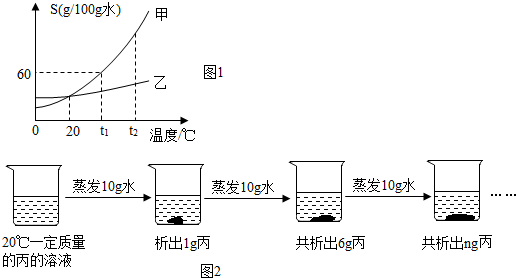
Ⅰ.在20℃时,甲和乙两种物质的溶解度相等.
Ⅱ.t1℃时,将50g固体甲加到50g水中,充分搅拌后所得溶液的质量为80g.
Ⅲ.甲的饱和溶液中含有少量的乙,由该液体得到固体甲采用的方法是降温结晶(或冷却热饱和溶液).
Ⅳ.若将甲物质的不饱和溶液变为饱和溶液,下列说法正确的是B.
A.溶剂的质量一定变小 B.溶质的质量可能不变
C.溶质的质量分数一定变大 D.溶液的质量变大
⑥图2是对20℃一定质量的丙溶液进行恒温蒸发结晶的实验过程,请回答:
Ⅰ.蒸发前原溶液是不饱和(填“饱和”或“不饱和”)溶液;m的数值是9.
Ⅱ.依据上述实验,你认为丙的溶解度随温度变化的趋势是C(填字母).
A.随温度升高而增大 B.随温度升高而减小 C.无法判断.
分析 ①根据二氧化碳和水反应生成碳酸解答;
②根据活性炭具有吸附性解答;
③根据铁丝在氧气中燃烧时的注意事项解答;
④粗盐提纯的实验步骤为溶解、过滤、蒸发,据此进行分析解答即可;
⑤根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;在t1℃时,甲、乙两物质的溶解度相等;t1℃时,甲的溶解度是60g,因此将50g甲投入到50g水中,充分搅拌后所得溶液的质量=30g+50g80g;要使接近饱和的乙溶液转化为饱和溶液,可以采用的方法是:增加溶质,蒸发溶剂,降低温度;
⑥根据饱和溶液的定义和判断方法进行分析;根据题中的数据以及题中析出晶体是通过蒸发溶剂得到的进行分析.
解答 解:①②二氧化碳和水反应生成碳酸,发生反应的化学方程式是:CO2+H2O=H2CO3
②自来水厂净水过程中常用到活性炭,其作用是吸附作用;
③铁丝在氧气中燃烧时,集气瓶内放少量水的目的是防止溅落的熔化物炸裂瓶底;
④粗盐提纯是通过溶解把不溶物与食盐初步分离,过滤把不溶物彻底除去,蒸发把食盐从溶液中分离出来而得到食盐的过程,其操作顺序应为溶解-过滤-蒸发.
在溶解、过滤、蒸发操作中都要用到的玻璃仪器是玻璃棒;
⑤Ⅰ.由溶解度曲线可知:在20℃时,甲、乙两物质的溶解度相等;
Ⅱ.t1℃时,甲的溶解度是60g,因此将50g甲投入到50g水中,充分搅拌后所得溶液的质量=30g+50g80g;
Ⅲ.甲的溶解度受温度影响较大,甲的饱和溶液中含有少量的乙,由该液体得到固体甲采用的方法是降温结晶(或冷却热饱和溶液);
Ⅳ.若将甲物质的不饱和溶液变为饱和溶液,
A、若采用的是降低温度至恰好饱和、增加溶质的方法,溶剂的质量不变,故选项说法错误.
B、若采用的是降低温度至恰好饱和,溶质的质量不变,故选项说法正确.
C、若采用的是降低温度至恰好饱和的方法,溶液的组成未发生改变,溶质的质量分数不变,故选项说法错误.
D、若采用的是降低温度至恰好饱和、蒸发溶剂的方法,溶液的质量分别会不变、减少,故选项说法错误.
⑥)Ⅰ蒸发前的烧杯底部没有固体,第一次蒸发10g水,析出1g晶体,第二次蒸发10g水析出5g-1g=4g晶体,所以蒸发前原溶液是不饱和溶液,第三次蒸发10g水析出4g晶体,所以共析出9g;故填:不饱和;9;
Ⅱ、题中析出晶体是通过蒸发溶剂得到的,不能判断出温度对溶解度的影响,故选:C.
答案:
(1)CO2+H2O=H2CO3;
(2)吸附作用;
(3)防止溅落的熔化物炸裂瓶底;
(4)过滤; 玻璃棒;
(5)20; 80; 降温结晶(或冷却热饱和溶液); B
(6)不饱和; 9; C.
点评 本题难度不大,熟练掌握粗盐的提纯的一般步骤、所需仪器等、掌握不饱和溶液变成饱和溶液一般采取三种方法(增加溶质、恒温蒸发溶剂、改变温度)是正确解答本题的关键.

 名校课堂系列答案
名校课堂系列答案| 温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(克) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,将15克硝酸钾放入50克水中,充分溶解,得到的溶液是不饱和(填饱和或不饱和)溶液,若20克硝酸钾放入50克水中,所得溶液中溶质的质量分数13%.
| A. | NH4NO3固体 | B. | 生石灰 | C. | 熟石灰 | D. | 食盐 |
| 浓硫酸(H2SO4)500ml | |
| 溶质的质量分数 | 60% |
| 密度 | 1.5g/cm3 |
(2)需要多少mL浓硫酸?
(3)在配制1000g质量分数为10%的稀硫酸中,需要多少mL水?
(4)如取10mL10%稀硫酸加水稀释至20mL,则所得稀硫酸的质量分数为多少?(假设在此过程中,溶液的密度变化可忽略)
 某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.
某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒. 某化学利用CuSO4、FeSO4的混合溶液进行如下探究实验.
某化学利用CuSO4、FeSO4的混合溶液进行如下探究实验.