题目内容
13. 在一烧杯中盛有26.4gNa2CO3和Na2SO4组成的固体混合物,加入80克水使其完全溶解,再向其中逐渐滴加溶质质量分数为10%的稀硫酸,放出气体的总质量与所滴入稀硫酸的质量关系如图所示,请根据题意计算:
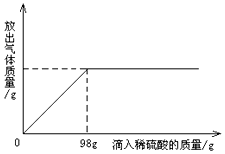
在一烧杯中盛有26.4gNa2CO3和Na2SO4组成的固体混合物,加入80克水使其完全溶解,再向其中逐渐滴加溶质质量分数为10%的稀硫酸,放出气体的总质量与所滴入稀硫酸的质量关系如图所示,请根据题意计算:(1)当滴加稀硫酸至恰好完全反应时,放出气体的总质量为多少克?
(2)原混合物中Na2CO3的质量分数是多少?(结果保留到0.1%)
(3)当恰好完全反应时,计算所得溶液中溶质的质量分数.
分析 (1)根据碳酸钠与稀硫酸反应,由反应的硫酸的质量求出生成的二氧化碳、硫酸钠的以及参见反应的碳酸钠的质量;
(2)根据碳酸钠的质量求出原混合物中Na2CO3的质量分数分析回答;
(3)根据溶质的质量分数的计算公式分析计算.
解答 解:(1)由图象可知,当加入稀硫酸的质量为98g时与碳酸钠恰好反应.
设Na2CO3的质量为x,生成的Na2SO4的质量为y,生成CO2的质量为z.
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 98 142 44
x 98g×10% y z
$\frac{106}{x}=\frac{98}{98g×10%}=\frac{142}{y}=\frac{44}{z}$
解得:x=10.6g y=14.2g z=4.4g
(2)原混合物中Na2CO3的质量分数=$\frac{10.6g}{26.4g}×100%$=40.2%.
(3)当恰好完全反应时,所得溶液中溶质的质量分数=$\frac{26.4g-10.6g+14.2g}{26.4g+80g+98g-4.4g}×100%$=15%
答:(1)当滴加稀硫酸至恰好完全反应时,放出气体的总质量为4.4g;
(2)原混合物中Na2CO3的质量分数是40.2%;
(3)当恰好完全反应时,计算所得溶液中溶质的质量分数为15%.
点评 本题难度较大,主要考查了根据化学方程式进行计算和有关溶液中溶质质量分数的计算,从而培养学生对概念的应用和分析问题、解决问题的能力.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
3.将25gA与5gB发生反应,所得混合物中含有10A,11gC,还有另外一种物质D.A、B、C、D相对质量分别为30、20、44、18,则它们之间反应的化学方程式正确的是( )
| A. | A+B=C+D | B. | 2A+B=2C+D | C. | 2A+B=C+2D | D. | A+2B=2C+D |
4.区分日常生活中的下列物质,所用方法不完全正确的是( )
| 需鉴别的物质 | 方法1 | 方法2 |
| A、一氧化碳和二氧化碳 | 分别通入澄清石灰水 | 分别通过灼热的氧化铜 |
| B、铁粉和木炭粉 | 看颜色 | 用磁铁吸引 |
| C、硬水和蒸馏水 | 加肥皂水 | 分别蒸干 |
| D、黄金和黄铜 | 分别加热 | 分别加入稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
18.下面说法正确的是( )
| A. | 取块状固体时可以用镊子或者纸槽 | B. | 空气中氧气的质量分数约为21% | ||
| C. | 氙气可以用作照相机的闪光灯 | D. | 试管、烧杯、量筒都可以用来加热 |
2.下列符号中,既能表示一种元素,又能表示该元素的一个原子,还能表示该元素所组成单质的是( )
| A. | O2 | B. | N | C. | Fe | D. | 2H |
3.下列关于“不一定”的说法中不正确的是( )
| A. | 软水不一定是纯水 | |
| B. | 纯净物不一定由同种分子构成 | |
| C. | 由同种元素组成的纯净物不一定是单质 | |
| D. | 能分解出氧气的化合物不一定是氧化物 |