题目内容
9.将16g高锰酸钾放入试管中加热,一会儿后停止加热,称得剩余固体的质量为14.4g,计算:(1)产生氧气的质量;
(2)剩余固体中高锰酸钾的质量分数.
分析 高锰酸钾受热分解后生成锰酸钾、二氧化锰和氧气,由于氧气逸出,所以反应后固体质量会减少;根据质量守恒定律可知,固体质量的减少量即为生成氧气的质量,然后根据反应方程式由氧气的质量求出参加反应的高锰酸钾及剩余的高锰酸钾和二氧化锰的质量.
解答 解:(1)由质量守恒定律可知,生成氧气的质量是:16g-14.4g=1.6g;
(2)设参加反应的KMnO4质量为x,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4 +MnO2 +O2↑
316 32
x 1.6g
则$\frac{316}{32}=\frac{x}{1.6g}$,解得:x=15.8g
剩余固体中未反应高锰酸钾的质量为:16g-15.8g=0.2g.
故剩余固体中高锰酸钾的质量分数为$\frac{0.2g}{14.4g}×100%$≈1.4%.
故答案为:1.6g;1.4%.
点评 此题考查的根据关化学方程式的计算,通过认真分析题干,直接得到氧气的质量,然后再求其他反应物的质量.此题计算量较大,计算一定要细心准确.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
19.甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
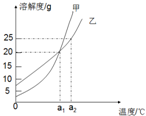

| A. | a1℃时,甲、乙溶液的浓度一定相等 | B. | a2℃时,乙的饱和溶液的浓度是20% | ||
| C. | 溶解度:甲>乙 | D. | 只能采用降温的方法获得甲晶体 |
17.水是生命之源,水的化学式为H2O,下列对水的认识正确的是( )
| A. | 水是由氢原子和氧原子构成 | B. | 水中氢、氧的质量比为2:1 | ||
| C. | 水中含有氧分子 | D. | 水由氢元素和氧元素组成 |
14.下列实验现象描述错误的是( )
| A. | 电解水时正极产生的氧气比负极产生的氢气多 | |
| B. | 白磷自燃产生大量的白烟 | |
| C. | 铝丝伸入硫酸铜溶液中铝丝表面有红色物质生成 | |
| D. | 铁丝在氧气中剧烈燃烧火星四射,产生黑色固体 |
18.小敏同学的化学复习笔记本上有如下记录,你认为正确的是( )
| A. | 化学反应发生时不一定能观察到明显的现象 | |
| B. | 从元素周期表中可以查出元素的相对原子质量 | |
| C. | 含有氧元素的化合物称为氧化物 | |
| D. | 书写化学方程式时,生成物中只要有气体生成就必须注明“↑”符号 |
19.为了探究“水的净化”过程,某实验小组从护城河中取了水样,观察到:
A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒
现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置沉淀一段时间后,进行 处理去固体小颗粒,再向所得液体中加入活性炭,利用其吸附性除去水样中的颜色和异味.
(2)通入氯气杀菌消毒,得到自来水,而K2FeO4物质既能净水又能杀菌,其中铁元素化合价为+6.
(3)使用硬水会给生活和生产带来许多麻烦,在日常生活中,我们常用煮沸方法来降低水的硬度,这个过程主要是将水中的可溶性钙盐转化为碳酸钙(水垢的主要成分)沉淀的过程.水垢过多锅炉易引起事故,请你写出除去水垢的有关化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.(除垢剂中有我们实验室常用的酸)
(4)如图所示的3个实验,A中水发生了物理(填“物理”或“化学”)变化;B试管2内得到的气体为氧气;C中小卵石、石英砂和蓬松棉的作用是过滤.
(5)矿泉水、蒸馏水有多种作用,例如:镁与碘的化合反应十分缓慢,若滴加少量水,则反应立即剧烈进行,反应速度大大提高,此时水的作用是催化剂.
A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒
现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置沉淀一段时间后,进行 处理去固体小颗粒,再向所得液体中加入活性炭,利用其吸附性除去水样中的颜色和异味.
(2)通入氯气杀菌消毒,得到自来水,而K2FeO4物质既能净水又能杀菌,其中铁元素化合价为+6.
(3)使用硬水会给生活和生产带来许多麻烦,在日常生活中,我们常用煮沸方法来降低水的硬度,这个过程主要是将水中的可溶性钙盐转化为碳酸钙(水垢的主要成分)沉淀的过程.水垢过多锅炉易引起事故,请你写出除去水垢的有关化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.(除垢剂中有我们实验室常用的酸)
(4)如图所示的3个实验,A中水发生了物理(填“物理”或“化学”)变化;B试管2内得到的气体为氧气;C中小卵石、石英砂和蓬松棉的作用是过滤.
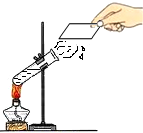 | 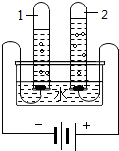 | 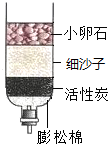 |
| A.水的沸腾 | B.水的电解 | C.水的净化 |
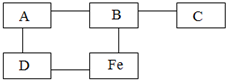 已知A、B、C、D分别是氧化铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液四种物质中的一种,它们以及Fe之间相互反应情况如图,“-”连接的两种物质能反应.请回答下列问题:
已知A、B、C、D分别是氧化铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液四种物质中的一种,它们以及Fe之间相互反应情况如图,“-”连接的两种物质能反应.请回答下列问题: