题目内容
9.工业上用22%~24%的稀硫酸清洗钢材后的废液称为酸洗液,酸洗液中含硫酸和硫酸亚铁,可用来生产铁红(氧化铁),其主要流程表示如下(其中溶液A中投加NaOH时发生复分解反应).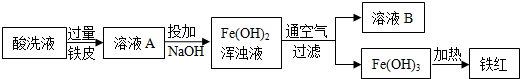
(1)酸洗液中加入铁皮反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(2)向Fe(OH)2浑浊液中通空气的目的是将Fe(OH)2转化为Fe(OH)3.
(3)溶液B中溶质一定含有Na2SO4.
分析 (1)根据铁和硫酸反应生成硫酸亚铁和氢气进行分析;
(2)根据氢氧化亚铁和氧气反应会生成氢氧化铁进行分析;
(3)根据氢氧化钠和硫酸亚铁反应生成氢氧化亚铁沉淀和硫酸钠进行分析.
解答 解:(1)铁和硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(2)氢氧化亚铁和氧气反应会生成氢氧化铁,所以向Fe(OH)2浑浊液中通空气的目的是:将Fe(OH)2转化为Fe(OH)3;
(3)氢氧化钠和硫酸亚铁反应生成氢氧化亚铁沉淀和硫酸钠,氢氧化亚铁和氧气反应会生成氢氧化铁沉淀,所以溶液B中溶质一定含有硫酸钠.
故答案为:(1)Fe+H2SO4=FeSO4+H2↑;
(2)将Fe(OH)2转化为Fe(OH)3;
(3)Na2SO4.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
4.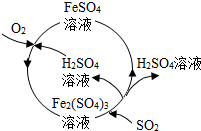 含硫煤燃烧会产生大气污染,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
含硫煤燃烧会产生大气污染,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
 含硫煤燃烧会产生大气污染,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
含硫煤燃烧会产生大气污染,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )| A. | 该过程中可得到化工产品H2SO4 | |
| B. | 该工艺流程是除去煤燃烧时产生的SO2 | |
| C. | 该过程中化合价发生改变的元素为Fe和S | |
| D. | 图中涉及到的反应之一为Fe2(SO4)3+SO2+2H2O═2FeSO4+2H2SO4 |
14.海南热带水果的种植带动了蜂蜜产业的发展.蜂蜜总含糖量达65%~75%,还含有丰富的酶类、水溶性维生素及钙、铁、锌等.则下列说法错误的是( )
| A. | 维生素可预防疾病、维持人体健康 | B. | 酶属于蛋白质 | ||
| C. | 蜂蜜的主要成分是糖类 | D. | 铁、锌、钙是人体必需的微量元素 |
18.下列内容是某同学对化学知识的归纳,其中不正确的是( )
| A. | 空气的组成:氮气、氧气、氢气、稀有气体等 | |
| B. | 燃烧需要三个条件:可燃物、氧气、温度达到着火点 | |
| C. | 常见的合成材料:塑料、合成纤维和合成橡胶等 | |
| D. | 人类所需要的六大基本营养素:蛋白质、糖类、油脂、维生素、无机盐和水 |
19.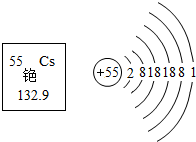 中国研制的铯原子钟,2000万年不差1秒,铯元素的部分信息如图所示.以下表述正确的是( )
中国研制的铯原子钟,2000万年不差1秒,铯元素的部分信息如图所示.以下表述正确的是( )
 中国研制的铯原子钟,2000万年不差1秒,铯元素的部分信息如图所示.以下表述正确的是( )
中国研制的铯原子钟,2000万年不差1秒,铯元素的部分信息如图所示.以下表述正确的是( )| A. | 铯是非金属元素 | B. | 铯的中子数为55 | ||
| C. | 铯的相对原子质量为132.9g | D. | 铯离子符号为Cs+ |
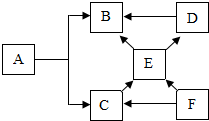 A-F是初中化学常见的六种物质,它们的转化关系如图所示.已知B是一种常见的液体,C可作补钙剂.D是一种单质,E是光合作用的原料.(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化),回答下列问题.
A-F是初中化学常见的六种物质,它们的转化关系如图所示.已知B是一种常见的液体,C可作补钙剂.D是一种单质,E是光合作用的原料.(部分反应物、产物及反应条件已略去,“→”表示物质之间能发生转化),回答下列问题.