题目内容
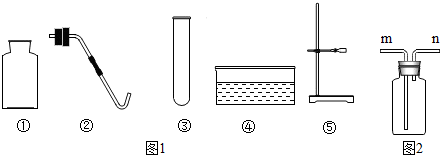
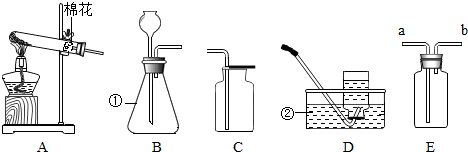
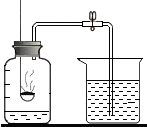 已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:(1)红磷在集气瓶中发生反应的现象:
(2)若未冷却到室温就打开止水夹,会导致测出的氧气含量偏
(3)已知:镁+氮气
| 点燃 |
| 点燃 |
考点:空气组成的测定
专题:空气与水
分析:(1)红磷在点燃条件下能和空气中的氧气反应生成五氧化二磷,产生大量白烟,放出大量的热;
(2)温度越高,气体的压强越大;
(3)镁能和空气中的多种物质发生化学反应,因此不能用作测定空气中氧气含量的物质.
(2)温度越高,气体的压强越大;
(3)镁能和空气中的多种物质发生化学反应,因此不能用作测定空气中氧气含量的物质.
解答:解:(1)红磷在集气瓶中发生反应时能够产生大量白烟,放出大量的热;
该实验中红磷需稍过量,其目的是使容器中的氧气完全反应.
故填:产生大量白烟,放热;保证瓶内氧气完全消耗.
(2)若未冷却到室温就打开止水夹,由于集气瓶中的温度很高,气体压强较大,会导致进入集气瓶中的水偏少,从而会导致测出的氧气含量偏低.
故填:低.
(3)不能用镁代替红磷测定空气中氧气的含量,这是因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应,这样进入集气瓶内水的体积必然大于氧气的体积,会导致测定的氧气含量偏高.
故填:不能;因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应,这样进入集气瓶内水的体积必然大于氧气的体积.
该实验中红磷需稍过量,其目的是使容器中的氧气完全反应.
故填:产生大量白烟,放热;保证瓶内氧气完全消耗.
(2)若未冷却到室温就打开止水夹,由于集气瓶中的温度很高,气体压强较大,会导致进入集气瓶中的水偏少,从而会导致测出的氧气含量偏低.
故填:低.
(3)不能用镁代替红磷测定空气中氧气的含量,这是因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应,这样进入集气瓶内水的体积必然大于氧气的体积,会导致测定的氧气含量偏高.
故填:不能;因为镁在空气中燃烧时,与氧气、二氧化碳和氮气都能够发生反应,这样进入集气瓶内水的体积必然大于氧气的体积.
点评:可以用来测定空气中氧气含量的物质应该具备的条件是:能和空气中的氧气反应,生成物是固体,不能和空气中的其它物质发生化学反应.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
民以食为天,厨房里的下列操作中,发生了化学变化的是( )
| A、将苹果晾成苹果干 |
| B、将大米酿成酒曲 |
| C、将面团擀成饺子皮 |
| D、将茄子切成小丁 |
在化学世界里没有生命的阿拉伯数字也变得鲜活起来.下列化学用语与所表述的意义不相符的是( )
| A、N2--氮气中氮元素的化合价为0 | ||
| B、3S--三个硫元素 | ||
| C、2H2O--2个水分子 | ||
D、4CO
|
 如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.